
题目列表(包括答案和解析)
2.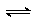 (8分) 在容积为1L的密闭容器中,充入1 mol N2和4 mol H2,一定条件下反应N2+3H2 2NH3 达到平衡,此时缓和体系中N2和H2的物质的量之比恰好为 1:5。试回答下列问题:
(8分) 在容积为1L的密闭容器中,充入1 mol N2和4 mol H2,一定条件下反应N2+3H2 2NH3 达到平衡,此时缓和体系中N2和H2的物质的量之比恰好为 1:5。试回答下列问题:
(1)平衡时混合气体的压强与起始时混合气体的压强相比 (填“偏高”、“偏低”或“相等”)。
(2)该平衡混合气中NH3的体积分数是 。
(3)通过计算,求达到平衡时H2的转化率为多少?
1.(8分)测定NaOH和Na2CO3的混合液中NaOH的含量时,可先在混合液中加入过量的BaCl2溶液,使Na2CO3完全变成BaCO3沉淀,然后用已知浓度的盐酸滴定(用酚酞作指示剂,其变色pH范围为8~10)。试回答:
(1)滴定时BaCO3能否不断溶解? (填“能” 或“不能”),理由是
;
(2)如用甲基橙作指示剂(其变色pH范围为3.1~4.4),则测定的结果 (填“偏高”、“偏低”或“无影响”)。原因是 。
2.(9分)在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,求达到平衡状态时,测得 c(H2)= 0.0080 mol·L-1
(1)则该反应的平衡常数K=_________ ____(填数值)。
(2)在上述温度下,该容器中若通入H2和I2各0.20mol 的气态混合物,求达到化学平衡状态时,各反应物的浓度是: [H2]= ________ mol·L-1, [HI]= ______________ mol·L-1。
1.(5分)将1molI2(g)和2molH2(g)置于2L密闭容器中,在一定
 温度下发生反应:
温度下发生反应:
 I2(g)+H2(g)
2HI(g) DH<0,并达到平衡。HI的体积分数j(HI) 随时间的变化如曲线(II)所示。
I2(g)+H2(g)
2HI(g) DH<0,并达到平衡。HI的体积分数j(HI) 随时间的变化如曲线(II)所示。
(1)达到平衡后,I2(g)的物质的量浓度为 ;
(2)若改变反应条件,在某条件下j(HI)的变化如曲线(Ⅰ)所示,则该条件可能是
(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当的催化剂
4.(6分)室温下,某水溶液中存在的离子有:Na+、A-、H+、OH-,据题意,回答下列问题。
①若由0.1mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合而得,则溶液的
pH 7(选填“大于或等于”、 “小于或等于”、 “等于”)。
②若溶液pH>7,则c (Na+) c(A-)(选填“>”、 “<”、 “=”)。
③若由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL。混合而得,则下列说法中,正确的是
(填选项符号字母)。
A.若反应后溶液呈中性,则反应后溶液中[H+]+ [OH-]=2×10-7mol·L-1
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
3.(4分)某温度时,在2L的密闭容器中,X、Y、Z三种物质的物
质的量随时间的变化曲线如图所示。
由图中所给数据进行分析,该反应的化学方程式为:
___________________________________________;
反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= _mol·L-1·min-1。
2.(4分)工业上由金红石(TiO2)制取单质Ti,涉及到的步骤为:
TiO2 →(步骤Ⅰ)TiCl4  (步骤Ⅱ)Ti
(步骤Ⅱ)Ti
(1)写出步骤Ⅱ中TiCl4→Ti的化学反应方程式 。
(2)已知:①C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) △H=+141kJ·mol-1
则反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H= kJ·mol-1。

1.(2分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2),当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应时,放出256kJ的热量。请写出该反应的热化学方程式:
________________________________________。
18.体积相同的甲、乙两个容器,分别都充等量的SO2和O2,在相同温度下发生反应:
2SO2(g)+O2(g) 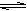 2SO3(g)并达到平衡,在此过程中,甲维持容器的体积不变,乙维持容器的压强不变,若甲中SO2的转化率为a%,则乙中SO2的转化率是转化率是下列的
( )
2SO3(g)并达到平衡,在此过程中,甲维持容器的体积不变,乙维持容器的压强不变,若甲中SO2的转化率为a%,则乙中SO2的转化率是转化率是下列的
( )
A.等于a% B.大于a% C.小于a% D.无法判断
高 二 化 学 试 题(B卷)
第Ⅱ卷 (非选择题 共46分)
17.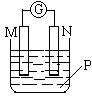 如右图所示装置中,可观察到电流计指针偏转,M棒变粗,N棒变细,
如右图所示装置中,可观察到电流计指针偏转,M棒变粗,N棒变细,
下表所列M、N、P物质中,可以组合成该装置的是( )
|
|
M |
N |
P |
|
A |
锌 |
铜 |
稀硫酸 |
|
B |
铜 |
铁 |
稀盐酸 |
|
C |
银 |
锌 |
 硝酸银溶液 硝酸银溶液 |
|
D |
锌 |
铁 |
硝酸铁溶液 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com