
题目列表(包括答案和解析)
24.(6分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
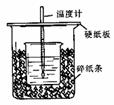 (1)从实验装置上看,图中尚缺少的一种玻璃用品是
。
(1)从实验装置上看,图中尚缺少的一种玻璃用品是
。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
23.(12分)有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒
压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1
的SO2和O2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下
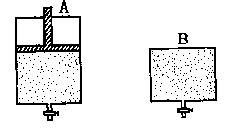 使之发生如下反应:2SO2+O2
使之发生如下反应:2SO2+O2 2SO3。试填写下列空格:
2SO3。试填写下列空格:
(1)A容器达到平衡时所需的时间比B容器_________;平衡时A容器中SO2的转化率比B容器_______;
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等物质的量的氩气,A容器中化学平衡__________________移动,B容器中化学平衡_______________移动;
(3)达到(1)所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数_________(填“增大”、“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数_________。
22.(8分)对于反应aA(g)+bB(g) cC(g)+dD(g),反应达平衡时,瞬时速率v(正)=k1·ca(A)·cb(B)
cC(g)+dD(g),反应达平衡时,瞬时速率v(正)=k1·ca(A)·cb(B)
(k1为速率常数),达平衡时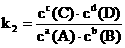 (k2为化学平衡常数),且k1、k2只与温度有关。现将4 mol SO2和2 mol O2充入容器为2 L的密闭容器中,500℃进行反应并保持温度不变,反应达到平衡时,SO2转化率为50%,则:
(k2为化学平衡常数),且k1、k2只与温度有关。现将4 mol SO2和2 mol O2充入容器为2 L的密闭容器中,500℃进行反应并保持温度不变,反应达到平衡时,SO2转化率为50%,则:
(1)起始时正反应速率是平衡时的 倍。
(2)在500℃时该反应的平衡常数k2是 。
(3)在温度不变时再向平衡体系中加入2 mol SO2,2mol O2和4 mol SO3,平衡将向
移动。(填“正反应方向”或“逆反应方向”)
21.(3分)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
_________________
20. 已知可逆反应aA+bB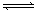 cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
A、该反应在T1、T3温度时达到过化学平衡
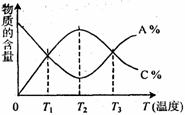 B、该反应在T2温度时达到过化学平衡
B、该反应在T2温度时达到过化学平衡
C、该反应的逆反应是吸热反应
D、升高温度,平衡会向正反应方向移动
第二卷(非选择题 共50分)
19、某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);(正反应放热)
2Z(g);(正反应放热)
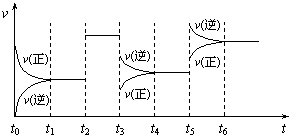
上图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4-t5时间内转化率最低
18.在1L密闭容器中通入2mol氨气,在一定温度下发生反应;2NH3  N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a
%的是
N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a
%的是
A.6mol H2和2mol N2 B.2mol NH3和1mol N2
C.2mol N2和3mol H2 D.0.1mol NH3、0.95mol N2、2.85mol H2
17. 向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g) 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
⑤其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A.①②③ B.①③⑤ C.②④⑤ D.①③④
16. 在一定条件下,固定容积的密闭容器中反应:2NO2(g)
在一定条件下,固定容积的密闭容器中反应:2NO2(g)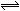 O2(g) + 2NO(g);(正反应吸热), 达平衡。改变其中一个条件X,Y随X变化符合曲线的是
O2(g) + 2NO(g);(正反应吸热), 达平衡。改变其中一个条件X,Y随X变化符合曲线的是
A.当X表示温度时,Y表示NO2的物质的量
B.当X表示温度时,Y表示NO2的转化率
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示NO2的物质的量时,Y表示O2的物质的量
15. 在恒温时,一固定压强的容器内发生如下反应:2NO2(g) 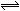 N2O4(g),达平衡是,再向容器内通一定量的NO2(g),重达平衡后,与第一次平衡时相比,NO2的体积分数
N2O4(g),达平衡是,再向容器内通一定量的NO2(g),重达平衡后,与第一次平衡时相比,NO2的体积分数
A、不变 B、增大 C、减小 D、无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com