
题目列表(包括答案和解析)
7.有镁、铝混合粉末10.2g,将它溶于500mL 4mol/L的盐酸里,若要使沉淀质量达到最大值,则需加入2 mol/L氢氧化钠溶液的体积为
A.100ml B.500ml C.1000ml D.1500ml
6.已知0.1mol·L-1的醋酸溶液中存在电离平衡CH3COOH CH3COO-+H+,要使溶液中c(H+) /c (CH3COOH)的值增大,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+) /c (CH3COOH)的值增大,可以采取的措施是
A.加入少量的烧碱溶液 B.降低温度
C.加入少量纯醋酸 D.加水
5.下列叙述正确的是
A.强电解质溶液的导电能力一定比弱电解质强
B.相同体积和PH的盐酸和醋酸与足量镁反应,放出氢气的体积相同
C.足量锌分别和等体积、等物质的量浓度的盐酸和醋酸反应,产生氢气的量相等,放出氢气的速率不等
D.物质的量浓度相同的磷酸钠和磷酸溶液中,c(PO43-)相同
4.可以表明合成氨反应:N2+3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
 A. 1个N N键断裂的同时,有3个H-H键形成
A. 1个N N键断裂的同时,有3个H-H键形成
 B. 1个N N键断裂的同时,有3个H- H键断裂
B. 1个N N键断裂的同时,有3个H- H键断裂
C. 3个H-H键断裂的同时,有6个N-H键形成
 D. 1个N N键断裂的同时,有6个N-H键形成
D. 1个N N键断裂的同时,有6个N-H键形成
3.下列关于化学反应速率的说法正确的是
A.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
B.化学反应速率0.8mol/(L·s)是指1s时某物质的浓度为0.8mol/L
C.根据反应速率的大小可以知道化学反应进行的快慢
D.对于化学反应来说,反应速率越大,反应现象越明显
2.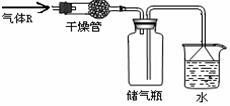 实验室里可按如右图所示的装置干燥、储存气
实验室里可按如右图所示的装置干燥、储存气
体R,多余的气体可用水吸收,则R是
A.NO2 B.HCl
C.CH4 D.NH3
1.H-可与NH3发生如下反应:H-+NH3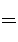
 NH2-+H2,据此可以说明
NH2-+H2,据此可以说明
A.NH3具有还原性 B.H-作还原剂
C.该反应是置换反应 D.该反应不是氧化还原反应
27.将0.05mol/L的盐酸溶液和未知浓度的NaOH溶液按1∶2体积比混合,所得混合液A的pH=12。用上述NaOH溶液滴定20mL pH=3的某一元弱酸溶液,达到滴定终点时消耗12.5 mL NaOH溶液。求:(1)NaOH溶液的物质的量浓度。(2)一元弱酸的物质的量浓度。
25.(4分)(1)图I表示10mL量筒中液面的位置,A与B,B与C刻
度相差1mL,如果刻度A为6,量筒中液体的体积是___________mL。
(2)图II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_____________。
A.是a mL B.是(50-a)mL C.一定大于a D.一定大于(50-a)mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com