
题目列表(包括答案和解析)
32.(6分)一种澄清透明的溶液中可能含有下列离子:
K+、Fe3+、Ba2+、Al3+、Cl-、I-、NO3-、HCO3-、SO32-、SO42-现做以下实验:
⑴将溶液滴在蓝色石蕊试纸上,试纸呈红色
⑵取少量溶液,加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀
⑶将⑵中的沉淀过滤。由滤液中加入硝酸银溶液,产生白色沉淀
⑷另取溶液,逐滴加入氢氧化钠溶液至过量,只观察到有红棕色沉淀生成,且沉淀量不减少。由此可以推断:
溶液中肯定存在的离子有: 。
溶液中肯定不存在的离子有: 。
溶液中还不能确定是否存在的离子有: 。
31. (8分)用已知物质的量浓度的盐酸滴定未知物质的量浓度的NaOH溶液(甲基橙作指示剂),试说明下列情况会使测定结果偏高、偏低还是无影响?
(1)用量筒量取待测液时,仰视读数;( )
(2)用碱式滴定管量取待测液,停止放液时,俯视读数;( )
( 3)记录起始体积时,仰视读数.终点时平视;( )
(4)滴定前,酸式滴定管无气泡,滴定后产生气泡;( )
30.(4分)如图
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为4,量筒中液体体积是
mL。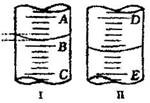
(2)图II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(50-a)mL
C.一定大于a mL D.一定大于(50-a)mL
29.(4分)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)== 1.8×10-10,Ksp(AgY)== 1.0×10-12,Ksp(AgZ)== 8.7×10-17;
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液 表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)
(填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为 (4)由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化?_______(填“能”或“不能”)。
28.(10分)在室温下,下列五种溶液:
①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4 ③ 0.1mol/L NH4HSO4
④0.1mol/L NH3•H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3•H2O
请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是
(用离子方程式表示)
(2)在上述五种溶液中,pH最小的是 ;c(NH4+)最小的是 ﹝填序号﹞
(3)比较溶液②、③中c(NH4+)的大小关系是② ③ ﹝填“>”、“<”或“=”)
(4)在溶液④中, 离子的浓度为0.1mol/L;NH3•H2O和 离子的物质的量浓度之和为0.2 mol/L
(5)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”、“<”或“=”) NH4+ 的水解程度,CH3COO-与NH4+浓度的大小关系是:
c(CH3COO-) c(NH4+)(填“>”、“<”或“=”)
27. (4分)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2 (s) Cu2+(aq)+2OH-(aq),常温下其Ksp=c(Cu2+) • c2(OH-)=2×10-20mol3•L-3。
(1))在室温下,某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于 。
(2)在室温下,要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。
26.(5分)在室温下,PH=2的某酸 HnA 与pH=12的某碱B(OH)m等体积混合,混合溶液的pH=8。
(1)反应生成正盐的化学式为 。
(2)该盐中 离子(填离子符号)一定能水解,其水解的离子方程式
为 。
25.(6分)下列物质中,能导电的是__________________,属于强电解质的是____________
属于非电解质的是________________(均填序号)
①Cu②液氨③氯水④氯化钠晶体⑤硫酸溶液⑥干冰⑦BaSO4⑧液氧⑨金刚石⑩石墨
24.在体积都为1L,pH ===2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是 ( )
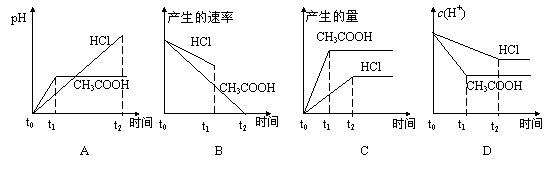
23.下列反应的离子方程式书写正确的是( )
A.向碘化亚铁溶液中通人足量的Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B.等物质的量的NaHCO3和Ba(OH)2在溶液中混合:
2HCO3-+Ba2++2OH- = BaCO3↓+2H2O+CO32-
C.向NaClO溶液中通人足量 SO2气体:2ClO-+SO2+H2O = SO32-+2HClO
D.将氨气通人硫酸氢钠溶液中:NH3+ H+ = NH4+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com