
题目列表(包括答案和解析)
26.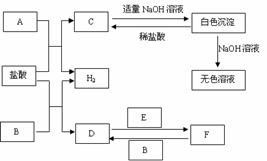 (5分)下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。
(5分)下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。
试回答下列问题:
(1)写出A与盐酸反应的离子方程式 。
(2)写出反应F→D的离子方程式是 。
(3)写出反应D→F的离子方程式是 。
(4)检验F中金属阳离子的常用试剂是 。
(5)工业上冶炼金属A的化学方程式是 。
25.(6分)为分析某县城的空气质量情况,某校化学研究性学习小组的同学拟测定该县城空气中SO2的含量。
⑴ 检验SO2可选用 试液。
⑵ SO2与酸性KMnO4溶液反应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+。该反应的现象是 ,SO2在该反应中显 (填“氧化”或“还原”)性。
⑶ 该小组的同学拟用下列装置运用“⑵”中的反应原理定量分析空气中SO2的含量:

① 装置中棉花的作用是 ,通入空气前应进行的实验操作是 ;
② 该实验中需要知道的数据除气体流速、酸性KMnO4溶液的体积外还有 。
24.(9分)Ⅰ我国采用食盐中加入碘酸钾(KIO3)的方法防止缺碘引起的疾病。
⑴在人体中,碘是属于 (选填“常量”或“微量”)元素;缺碘引起的疾病有 。
⑵已知在酸性溶液中IO3-可和I-发生反应:IO3-+5I-+6H+=3I2+3H2O,萃取碘水中的碘时,可选用的试剂是 ;利用上述反应,检验食盐中加入碘酸钾必须使用的物质是____________(可供选用的有:①自来水,②蓝色石蕊试纸,③碘化钾淀粉试纸,④淀粉,⑤食糖,⑥食醋)。
⑶已知碘酸钾受热易分解,在用碘酸钾加碘盐进行烹饪时应注意 。
II 近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。酸雨的特征是pH<5.6,空气中硫氧化物和氮氧化物是形成酸雨的主要物质。
(1) 酸雨落至地面后pH在一定时间内变小然后稳定于某一数值,原因是H2SO3受空气影响造成的,其化学方程式为:
(2)为了降低硫氧化物造成的空气污染,一种方法是在含硫燃料(如煤)燃烧过程中加入生石灰,这种方法叫“钙基固硫”,采用这种方法在燃料燃烧过程中的“固硫”反应为:_____________________ _ __
III生活处处有化学,化学与生产、生活密切相关。请回答:
(1)经科学测定,人体平均含氧65%,含碳18%,含氢10%(以上均为质量分数),则三种元素中原子数目最多的是 (填元素符号)。
(2)为验证某易拉罐材质的主要成分是铁制还是铝制,如用物理方法验证,一般用 即可;如用化学方法验证,可使用的化学试剂为 。
(3)据报道,全世界每年因金属腐蚀造成的直接经济损失约达7000亿美元,我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%。钢铁在潮湿的空气中发生电化学腐蚀时,负极的电极反应式为 。
(4)天然橡胶主要成分的结构简式是 。橡胶硫化的目的是使线型橡胶分子之间通过硫桥交联起来,形成 ,从而改善橡胶的性能。
23.下列说法正确的是
A.碳酸氢钠可作抗酸药,阿司匹林是重要的抗生素
B.玻璃钢广泛用于制造汽车车身、船体和印刷电路板
C. 为使火腿肠颜色更鲜红,可多加一些亚硝酸钠
D.人体缺少维生素A易患夜盲症、干眼症
第Ⅱ卷(非选择题 共31分)
22. 右图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。则该物质不具有的性质是
右图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。则该物质不具有的性质是
A.使紫色石蕊变红 B.与钠反应
C.发生酯化反应 D.发生氧化反应
21.下列有机物发生的反应属于加成反应的是
A.乙醇使KMnO4溶液褪色 B.乙烯使溴的四氯化碳溶液褪色
C.甲烷和氯气混合,见光 D.用乙醇、乙酸与浓H2SO4混合加热
20.下列对各物质性质的解释不正确的是
|
选项 |
性质 |
原因 |
|
A |
氯水的漂白性 |
氯气的强氧化性 |
|
B |
明矾用来净水 |
Al3+水解生成Al(OH)3胶体,具有吸附性 |
|
C |
苯燃烧有浓黑的烟 |
苯分子中含碳量较高 |
|
D |
加热铝箔,熔化的铝不滴落 |
铝表面的氧化膜熔点高,包在熔化的铝外面 |
19.下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
|
编号 |
金属(粉末状) |
物质的量 |
酸的浓度 |
酸的体积 |
反应温度 |
|
A |
Mg |
0.1mol |
6mol/L硝酸 |
10mL |
60℃ |
|
B |
Mg |
0.1mol |
3mol/L盐酸 |
10mL |
30℃ |
|
C |
Fe |
0.1mol |
3mol/L盐酸 |
10mL |
60℃ |
|
D |
Mg |
0.1mol |
3mol/L盐酸 |
10mL |
60℃ |
18.下列说法正确的是
A.化学反应中化学能只可以转化为热能
B.可逆反应达到平衡后,正、逆反应速率均为0
C.N2和H2反应达到平衡后,无N2或H2剩余
D.化学反应中一定有化学键的断裂和形成
17.X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物是强碱,Z
的原子半径最小。据此判断下列说法正确的是
A.X是第ⅠA元素,Z是第ⅦA元素
B.Y一定是金属元素
C.Z的最高价氧化物对应的水化物是弱酸 D.X、Z形成的化合物是共价化合物 学
学
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com