

题目列表(包括答案和解析)
7.下列物质属于芳香烃,但不是苯的同系物的是( )
①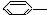 CH3 ②
CH3 ②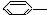 CH=CH2
③
CH=CH2
③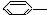 NO2
NO2
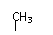
 ④
④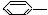 OH ⑤ ⑥
OH ⑤ ⑥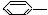 CH-CH2
CH-CH2
A.③④ B.②⑤ C.①②⑤⑥ D.②③④⑤⑥
6.用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为( )
A. 3种 B.4种 C. 5种 D.6种
5.以下命题,违背化学变化规律的是( )
A.石墨制成金刚石 B.煤加氢变成人造石油
C.水变成汽油 D.海水淡化可以缓解淡水危机
4.一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25。使混合气通过足量溴水,溴水增重8.4g,则混合气中的烃分别是( )
A.甲烷和乙烯 B. 甲烷和丙烯 C. 乙烷和乙烯 D. 乙烷和丙烯
3.制取一氯乙烷最好采用的方法是( )
A.乙烷和氯气反应 B.乙烯和氯气反应
C.乙烯和氯化氢反应 D.乙烷和氯化氢反应
2.下列分子中所有原子不可能共处在同一平面上的是( )
A. C2H2 B. CO2 C. NH3 D.C6H6
1.烯烃不可能具有的性质有( )
A.能使溴水褪色 B.加成反应 C.取代反应 D.能使酸性KMnO4溶液褪色
23.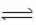 (7分)难溶电解质在水溶液里存在着电离平衡。在常温下,溶液里各离子浓度以它们的系数为方次的乘积是一个常数,该常数叫溶度积(Ksp)。例如FeS(s) Fe2+
(aq)+ S2-(aq) ,Ksp = c(Fe2+)·c(S2-) = 6.25×10-18 。溶液里各离子浓度幂的乘积,大于溶度积时则出现沉淀;反之沉淀溶解。试根据上述原理,计算:
(7分)难溶电解质在水溶液里存在着电离平衡。在常温下,溶液里各离子浓度以它们的系数为方次的乘积是一个常数,该常数叫溶度积(Ksp)。例如FeS(s) Fe2+
(aq)+ S2-(aq) ,Ksp = c(Fe2+)·c(S2-) = 6.25×10-18 。溶液里各离子浓度幂的乘积,大于溶度积时则出现沉淀;反之沉淀溶解。试根据上述原理,计算:
(1)求常温下FeS的溶解度( g/100g水)。(设饱和溶液的密度为1g.cm-3)
(2) 求常温下H2S的饱和溶液中,c(H+)与c(S2-)间存在关系有
[c (H+)]2·[c(S2-)]=1.0×10-22,在该温度下,将适量FeS投入H2S饱和溶液中,欲使溶液中c(Fe2+)达到1mol/L,应调节溶液的pH为多少?(已知:lg2≈0.3)
22.(10分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
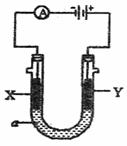
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中Y极上的电极反应式是 。
检验Y电极上电极反应产物的方法是____________________________________ _____________________________________________________。
②在X电极附近观察到的现象是_____________________________________________
________________________________________________________.
③要使电解后溶液恢复到电解前的状态,则需加入(或通人)___________________.
(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①Y电极的材料是 ;X电极反应式是 。
②电解完成后,硫酸铜溶液的浓度________________(填“变大”、“变小”、“不变”)
(3 )若X、Y都是铜电极,a是浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后X电极有3.2 g铜析出,此时直流电源已输出___________mol电子。
21.(9分)25℃时,将0.01molCH3COONa和0.002molHCl溶于水,形成1L混合溶液。
(1)该溶液中存在着 个平衡体系,用电离方程式或离子方程式表示:(可填满,也可不填满,如不够空,可以再加)
a.
b.
c.
(2)溶液中共有 种不同的粒子
(3)在这些粒子中,浓度为0.01mol/L的是 ,浓度为0.002mol/L的是 ;
(4) 和 两种粒子物质的量之和等于0.01mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com