
题目列表(包括答案和解析)
3、某种药物主要成分X的分子结构如下:
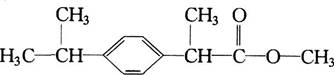
关于有机物X的说法中,错误的是 ( )
A.X难溶于水,易溶于有机溶剂 B.X能跟溴水反应
C.X能使酸性高锰酸钾溶液褪色 D.X的水解产物能发生消去反应
2、2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为( )
A、5种 B、4种 C、3 种 D、2种
1、下列取代基或微粒中,碳原子都满足最外层为8电子结构的是( )
A.乙基(-CH2CH3) B.碳正离子[(CH3)3C+]
C.碳化钙 (CaC2) D.碳烯 (:CH2)
20、(8分)
向10ml 2mol/L的AlCl3溶液中,加入lmol/L的NaOH溶液,当生成沉淀0.78 g时,加入的NaOH溶液的体积可能是多少ml?
附加题
(大同一中、大同二中、同煤一中、浑源中学、阳高一中的考生必做,其它学校自愿)
某二元酸H2A在水中的电离方程式是H2A=H++HA- HA-DH++A2-
回答下列问题:
(1)Na2A溶液显 性(填“酸”、“中”或“碱”),理由是:(用离子方程式表示)
(2)若0.1mol·L-1 NaHA溶液的PH=2,则0.1mol·L-1H2A溶液中的氢离子的物质的量浓度可能是 0.11mol·L-1 (填“>”、“<”、“=”)理由是
(3) 0.1mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是
2008-2009学年度第一学期期末教学质量检测
19、(15分)
某兴趣小组在研究性学习中设计了如下实验:探究Fe与H2s0。反应的过程,装置如匿

 所示。实验步骤和实验现象如下:
所示。实验步骤和实验现象如下:
①在烧瓶中加入80%的H2SO4溶液
②将提拉式银白色铁丝伸入溶液中,片刻伸部分铁丝变黑后停止了现象。
③加热烧瓶有大量气体产生,品红溶液褪色,烧瓶中溶液变成棕黄色。
④一段时间后,KMnO4溶液颜色不再变浅,但NaOH溶液中仍有气泡逸出,在导管处点燃气体,火焰呈淡蓝色,烧瓶中液体变为浅绿色。
(1)步骤②中的现象说明
(2)步骤③中烧瓶内的化学反应方程式
(3涉骤④中烧瓶内发生反应的离子方程式
(4)利用下表完成设计实验:证明反应完成后,烧瓶中的溶液有Fe2+。
|
实验操作 |
实验现象 |
有关反应的离子方程式 |
|
|
|
|
18、(16分)
(A)A、B两种有机物都能使溴水褪色,在催化剂条件下与过量的H。充分反应都能生成
2一甲基丁烷;0.4 mol的A或0.4mol的B都可以和128g Br2完全反应,A生成物c中的Br原子分布在4个碳原子上,B生成物D中的Br原子分布在2个碳原子上。
(1)写出A、B的结构简式A B
(2)完成反应方程式:A+ Br2→C
B + Br2→D
(3命名:生成物C的名称为
(4)写A与B具有相同官能团的B的同分异构体
(B)(16分)
A、B、C、D、E五种溶液,它们的阳离子分别是Ag+、Na+、Ba2+、Al3+、Fe3+,阴离子分别是Cl-、NO3-、OH-、SO42-,、CO32-(离子没有重复的)。
已知①C溶液加入铁粉,溶液质量增加。
②A、E溶液都呈碱性,且0.1mol的A溶液PH小于13。
③B溶液中逐滴加入氨水,出现沉淀,继续加入氨水沉淀消失
④D溶液中加入B a(NO3)2无现象。
(1)写出A、B、C、D、E的化学式
A 、B 、C 、D 、E
(2)完成下列溶液混合时的离子反应方程式
A与D混合
C与E混合
17、(7分)如不慎把白磷沾在皮肤上,可立即片CuSO4溶液冲洗,发生的化学反应为:

(1)配平上化学反应方程式并标出电子得失情况
(2)该反应中 是氧化剂, 是氧化产物
16、(9分)
在一定温度下,冰醋酸加水稀释的过程中,溶液的导电性如图。请回答:
(1)“O”点时导电能力为O的理由
 (2)a、b、c三点溶液中c(H-)由小到大的顺序为
(2)a、b、c三点溶液中c(H-)由小到大的顺序为
(3)若用润湿的PH试纸测定a点的PH,所测PH与实
际相比 (填“偏大”、“偏小”或“不变”)
(4)若使c点的溶液c(CH3COO-)增大,溶液的PH也增
大,可采用的措施是
①
②
③
15、 2008年北京奥运会期间,作为马拉松领跑车和电视拍摄车使用的是我国自行生产的燃料电池汽车。体现了“绿色奥运”、“科技奥运”。该质子交换燃料电池的T作原理如图,下列叙述不正确的是
2008年北京奥运会期间,作为马拉松领跑车和电视拍摄车使用的是我国自行生产的燃料电池汽车。体现了“绿色奥运”、“科技奥运”。该质子交换燃料电池的T作原理如图,下列叙述不正确的是
A正极反应式:O2+4H++4e-=2H2O
B负极反应式:2H2-4e-=4H+
c H+在电池内部由正极通过质子交换膜移动到负极
D总反应方程式:2H2+O2=2H2O
第Ⅱ卷(非选择题,共55分)
14、下列反应离子方程式正确的是
A碳酸钠溶液届碱性:
B碳酸氢钠溶液与过量石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
c钠与冷水反应:Na+2H2O=Na++H2↑+2OH-
D碳酸氢铵溶液与过量的氢氧化钠溶液: HCO3-+OH- = CO32-+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com