
题目列表(包括答案和解析)
(二)有机化学基础
24.(6分)18世纪,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式为: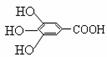 。
。
(1)用没食子酸制造墨水主要利用了__________类化合物的性质(填代号)。
A、醇 B、酚 C、油脂 D、羧酸
(2)没食子酸丙酯且有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为_______________________________________ 。
(3)写出没食子酸丙酯与氢氧化钠溶液反应的化学方程式:
。
25.(5分)已知有机物A、B、C、D、E都是常见的烃的含氧衍生物,C的相对分子质量为60,D是最简单的醇,E是酯。它们之间有下图所示的转化关系:
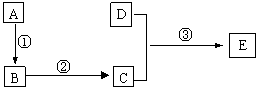

请根据上图回答:
⑴ D的分子式为 ;
⑵ 属于取代反应的是(填序号) ;
⑶ 写出与E互为同分异构体且属于酯的有机物结构简式: ;
⑷ 写出A在Cu或Ag催化下与O2反应的化学方程式: 。
26.(4分)BAD(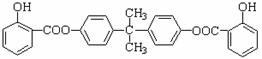 )是一种紫外线吸收剂。请回答下列问题:
)是一种紫外线吸收剂。请回答下列问题:
(1)预测该物质可能发生的反应( )
A. 能与浓溴水反应 B. 能发生加成反应 C. 能发生水解 D. 能发生氧化反应
(2)该物质苯环上的一氯取代物的种类有 种。
1.一种“即食即热型”快餐适合外出旅行时使用。它是利用两种物质发生化学反应对食物进行加热,这两种化学物质最合适的选择是
A.浓硫酸与水 B. 生石灰与水 C. 熟石灰与水 D. 氯化钠与水
2.下列各组物质的名称描述正确的是
A.酸:凡是能够电离出H+的化合物 B.碱:凡是能够电离出OH-的化合物
C.盐:金属阳离子(或相当于金属阳离子)和酸根离子组成的化合物
D.氧化物:凡是含有氧元素的化合物
3.下列物质能用分液的方法进行分离的是
A. 汽油和煤油 B. 乙醇和水
C. 乙酸和乙醇 D. 乙酸乙酯和饱和的碳酸钠溶液
4.下列表示化学用语或模型正确的是
A.8个中子的碳原子的核素符号:12C
B.H2O的电子式:
C.Cl-离子的结构示意图: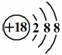 D.CH4分子的比例模型:
D.CH4分子的比例模型:
5.实验室用98%的浓硫酸(密度为1.84g/mL)配置500 mL 0.5 mol/L的稀硫酸。选用的主要仪器烧杯、胶头滴管、玻璃棒中,还缺少
A.容量瓶、13.6 mL量筒 B.500 mL容量瓶、100 mL量筒
C.容量瓶、100 mL量筒 D.500 mL容量瓶、25 mL量筒
6.下列有关物质的性质或用途的叙述中,错误的是
A.硅晶体是一种重要的半导体材料 B.石灰石是制备玻璃、水泥等工业的原料之一
C.石墨可用做绝缘材料
D.常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车
7.具有漂白作用的物质:①氯气;②二氧化硫;③活性炭;④过氧化钠,其中漂白原理相同的是
A.①③ B.②③ C.①④ D.②④
8.设NA为阿伏加德罗常数,下列说法中正确的是:
A.在常温常压下,11.2 L氮气所含有的原子数目为NA
B.活泼金属从盐酸中置换出1 mol H2,电子转移数为NA
C.500 mL 0.5mol/L Al2(SO4)3溶液中,SO42-的浓度为1.5 mol·L-1
 D.1.7 g 氨气所含的电子数目为 10 NA
D.1.7 g 氨气所含的电子数目为 10 NA
9.右图是制取和收集某气体的实验装置,该装置可用于
A.浓盐酸和二氧化锰反应制取Cl2
B.浓氨水和生石灰反应制取NH3
C.浓硝酸与铜反应制取NO2
D.二氧化锰固体和双氧水反应制取O2
10.对下列有机反应类型的认识中,错误的是
A.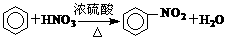 ;取代反应
;取代反应
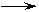 B.CH2=CH2
+ Br2
CH2Br-CH2 Br
;加成反应
B.CH2=CH2
+ Br2
CH2Br-CH2 Br
;加成反应
C.CH4 + Cl2 CH3Cl + HCl ;置换反应
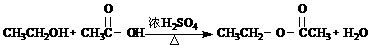
D. ;酯化反应
11.下列离子方程式书写正确的是
A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2↑+ H2O
B.铁和稀硝酸反应:Fe + 2H+ = H 2↑+ Fe 2+
 C.向AlCl3溶液中加入过量的NaOH溶液:Al3+ + 3OH- = Al(OH)3↓
C.向AlCl3溶液中加入过量的NaOH溶液:Al3+ + 3OH- = Al(OH)3↓
D.用氢氧化钠检验氯化铵溶液中铵根离子:NH4+ + OH― NH3 ↑+ H2O
12.下列化学反应属于吸热反应的是
A.碘的升华 B.浓硫酸溶于水
C.镁在氮气中燃烧 D.氢氧化钙与氯化铵晶体混合
13.为了验证碳酸氢钠固体中是否含有碳酸钠。下列实验及判断中,正确的是
A.加热,观察是否有气体放出 B.溶于水后加石灰水,看有无沉淀
C.取少量配成稀溶液滴加氯化钡溶液,看有无沉淀
D.加热后称量,看质量是否变化
14.在碱性条件下,由经过处理的工业级硫酸亚铁和氢氧化钠通过氧化沉淀的方法,可以制备适合复印墨粉用高档四氧化三铁磁粉。则四氧化三铁和三氧化二铁属于
A.同素异形体 B.同位素 C.同分异构体 D.同一金属的不同氧化物
15.关于化学键的叙述中,正确的是
A.离子化合物可能含共价键 B.共价化合物可能含离子键
C.离子化合物中只含离子键 D.离子化合物中一定含有金属离子
16.X、Y、Z都是第三周期元素,核电荷数依次增大,Z的最高价氧化物对应水化物的酸性最强,X的一种单质着火点仅40℃。据此判断下列说法不正确的是
A. X是第ⅤA元素,Z是第ⅦA元素 B. X、Y、Z三种元素的最高化合价逐渐减小
C. Y的最高价氧化物对应的水化物是强酸 D. X、Z形成的化合物是离子化合物
17.下列过程应用于工业生产的是
A.钠在氯气中燃烧制氯化钠 B.氯化铵与氢氧化钙共热制氨气
C.浓盐酸与二氧化锰共热制氯气 D.氯气与石灰乳反应制漂白粉
18.在下列三个反应中,过氧化氢(H2O2)所起的作用是
①H2O2+H2S==2H2O+S↓ ②2H2O2 MnO2====== 2H2O+O2↑ ③H2O2+Cl2==2HCl+O2↑
A.均起氧化剂作用 B.均起还原剂作用
C.均既是氧化剂又是还原剂 D.三个反应中所起作用各有不同
19.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:(1)a、c均能与稀硫酸反应放出气体;(2)b与d的硝酸盐反应,置换出单质d;(3)c与强碱溶液反应放出气体;(4)c、e在冷的浓硫酸中发生钝化。由此可判断a、b、c、d、e依次为
A.Fe Cu Al Ag Mg B.Al Cu Mg Ag Fe
C.Mg Cu Al Ag Fe D.Mg Ag Al Cu Fe
20.一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生。下列有关说法正确的是
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,正反应和逆反应的速率都为零
D.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
21.某无色溶液能与铝反应放出氢气,该溶液中肯定不能大量共存的离子组是
A.Na+、Fe2+、SO42-、K+ B.HCO3-、K+、NO3-、SO42-
C.SO42-、Cl-、CO32-、Na+ D.NH4+、Cl-、Na+、Ba2+
22.对于某些离子的检验及结论正确的是
A.加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中一定有CO32-
B.加氯化钡溶液有白色沉淀产生,再加盐酸,淀淀不消失,原溶液中一定有SO42-
C.加氢氧化钠溶液加热产生的气体使湿润红色石蕊试纸变蓝,原溶液中一定有NH4+
D.加入NaOH后溶液中产生白色沉淀,原溶液中一定有Mg2+
23.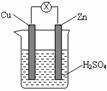 如右图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。下列叙述正确的是
如右图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。下列叙述正确的是
A.Zn是负极,发生还原反应
B.电子从锌片经外电路流向铜片
C.一段时间后溶液变蓝
D.铜片上可见气泡,一段时间后溶液总质量减少

 (3)人们熟知的一种感冒药阿司匹林的结构式为:
(3)人们熟知的一种感冒药阿司匹林的结构式为:
请你写出其中含有的一种官能团的名称 。
26. (4分)汽车尾气(含有烃类.CO.SO2与NO等物质)是城市的污染源。治理的方法之一是在汽
车的排气管上装一个“催化转换器”(用铂.钯合金作催化剂)。它的特点是使CO与NO
反应,生成无毒气体,并促使烃类充分燃烧及SO2的氧化。写出NO分别与CO、SO2
反应的化学方程式:
, 。
36、(15分)实验室用燃烧法测定某种α-氨基酸X (CxHyOzNp)的分子组成。取1.67 g X放在纯氧中充分燃烧,生成CO2、H2O和N2。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题:
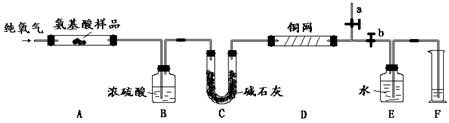
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通一段时间的纯氧,这样做的目的是 ;之后则需关闭止水夹 ,打开止水夹 。
(2)以上装置中需要加热的有(填装置代号) 。操作时应先点燃 处的酒精灯。
(3)装置A中发生反应的化学方程式为
CxHyOzNp+
O2 CO2+ H2O+ N2
CO2+ H2O+ N2
(4)装置D的作用是 ;
(5)读取N2所排水的体积时,要注意:① ;② 。
(6)实验中测得N2的体积为V mL(已换算成标准状况)。为确定此氨基酸的分子式,还需得到的数据有(填字母) 。
A.生成二氧化碳气体的质量 B.生成水的质量 C.通入氧气的体积 D.该氨基酸的摩尔质量
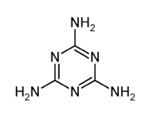 (7)三鹿问题奶粉就是不法分子利用上述原理在兑水的牛奶中加入了三聚氰胺以增加含氮量,计算三聚氰胺中氮元素的质量分数为____________ 。
(7)三鹿问题奶粉就是不法分子利用上述原理在兑水的牛奶中加入了三聚氰胺以增加含氮量,计算三聚氰胺中氮元素的质量分数为____________ 。
2008-2009学年度第二学期期中考试
35.(14分)A.B.C.D四种芳香族化合物的结构简式如下所示:

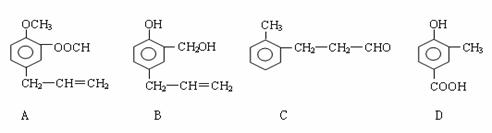
请回答下列问题:
(1)写出A中无氧官能团的名称 ,D中含氧官能团的结构简式为 。
(2)用A.B.C.D填空:能发生银镜反应的有 ,既能与FeCl3溶液发生显色反应又能与Na2CO3溶液反应放出气体的是 。
(3)按下图C经一步反应可生成E,E是B的同分异构体,
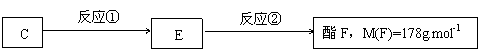
则反应①的反应类型为 ,写出反应②的化学方程式: 。
(4)G.H和D互为同分异构体,它们具有如下特点:
① G和H都是苯二元取代物,这两个取代基分别为羟基和含有-COO-结构的基团;
② G和H苯环上的一氯代物有两种不同结构;
③ G可以发生银镜反应,H分子中苯环不与取代基碳原子直接相连 。
写出G和H的结构简式:G: ;H: 。
34.(11分)A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A、E在周期表中处于同一纵行.已知:①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;②A与B,B与D都能生成非极性分子,B与C生成的气态非极性分子为直线型分子;③D与E生成离子化合物,其离子的电子层结构相同.回答:
(1)A为____ 元素,B为____ 元素,E为_____ 元素(填名称)
(2)C元素在周期表中属第________周期,第________族元素;
(3)B与C形成的化合物的电子式__ __,其固态时俗名 ,属________ 晶体;
(4)C与E形成的化合物的电子式为____________和____________,属______ 晶体.
33.(5分)某有机物A分子式为CxHyOz,15gA完全燃烧生成22gCO2和9gH2O。
(1)求该有机物的最简式
(2)若A是一种无色具有强烈刺激气味的气体,具有还原性,则其结构简式是_____________。
(3)若A和Na2CO3混合有气体放出,和醇发生酯化反应,则A的结构简式为:_________。
(4)若A是易挥发有水果香味的液体,能发生水解的反应,则其结构简式为:___________。
(5)若其分子结构中含有6个碳原子,具有多元醇和醛基的性质,则其结构简式为____________。
32.(8分)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3=Cu(NO3)2+NO↑+NO2↑+H2O。
(1) 硝酸在该反应中的作用是 ,该反应的还原产物是 。
(2) 0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是 ,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是 ,若用排水法收集这些气体,可得标准状况下的气体体积 。
(3) 如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式_____________________________________________________________。
30.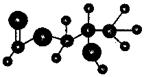 某有机物含有C、H、O三种元素,其球棍模型如图所示。该有机物可能发生的反应有
某有机物含有C、H、O三种元素,其球棍模型如图所示。该有机物可能发生的反应有
①水解 ②加聚 ③取代 ④消去 ⑤银镜
A.①③④ B.①④⑤
C.①②③④⑤ D.①③④⑤
第Ⅱ卷(非选择题,共60分)
31(7分)(1)用平行可见光照射肥皂水,从侧面可以见到光亮的通路。这种现象称为
(2)将饱和FeCl3溶液滴入沸水中可得红褐色液体,反应的离子方程式是 用半透膜把制取的Fe(OH)3胶体中含有的FeCl3和HCl分离出去的方法叫做 _,在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做_ 。
(3)油脂皂化后,使肥皂和甘油充分分离,可以采用的方法是
29.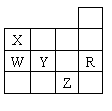 右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.Y元素的氢化物比W元素的氢化物稳定
D.X的氢化物沸点比W的氢化物的沸点高
28.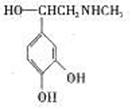 肾上腺素可用于支气管哮喘过敏性反应,其结构简式如下。下列关于肾上腺素的叙述正确的是
肾上腺素可用于支气管哮喘过敏性反应,其结构简式如下。下列关于肾上腺素的叙述正确的是
A.该物质的分子式为C9H16NO3
B.该物质在强碱的醇溶液中可以发生消去反应
C.1mol该物质与NaOH溶液反应,可以消耗2mol NaOH
D.该物质与浓溴水既能发生取代反应,又能发生加成反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com