
题目列表(包括答案和解析)
5、下列有关化学用语正确的是( )
A、乙烯的最简式C2H4
B、乙醇的结构简式C2H6O
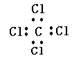
C、四氯化碳的电子式 D、臭氧的分子式O3
4、下列反应属于取代反应的是( )
A、乙醇与浓硫酸共热到170℃ B、乙醇与乙酸反应生成乙酸乙酯
C、乙醇与氧气反应生成乙醛 D、乙醇在空气中燃烧
3、将下列物质分别加入水中,振荡后静置,能分层且浮于水面上的是( )
A、溴苯 B、汽油 C、硝基苯 D、乙酸
2、近期我国冀东渤海湾发现储量达10亿吨的大型油田。下列关于石油的说法正确的是( )
A、石油属于可再生矿物能源 B、石油主要含有碳、氢两种元素
C、石油的裂化是物理变化 D、石油分馏的各馏分均是纯净物
1、 下列物质中,具有固定沸点的是( )
A、食醋 B、福尔马林 C、石炭酸 D、汽油
15.(10分)为了更好地表示溶液的酸碱性,有人建议用AG表示溶液的酸度,AG的定义为AG=lgc(H+)/c(OH-)。试计算:
(1)25℃,某呈中性溶液的AG;
(2)25℃,某pH=5的溶液的AG;
(3)试写出25℃时,溶液的pH与AG的换算公式。
14.(14分)密闭容器中,保持一定温度,进行如下反应:N2(g)+3H2(g)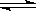 2NH3(g)。
2NH3(g)。
已知加入1mol N2和3mol H2,在恒压条件下,达到平衡时生成amol NH3[见下表中编号(1)的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,达到平衡时混合物中各组分的百分含量不变,请填空:
|
状状 条件 |
起始时各物的物质的量(mol) |
平衡时NH3的物质量的量 (mol) |
||||
|
编号 |
x(N2) |
y(H2) |
z(NH3) |
|||
|
恒 压 |
(1) |
1 |
3 |
0 |
a |
|
|
(2) |
3 |
|
0 |
|
||
|
(3) |
|
|
0.2 |
0.5a |
||
|
x、y、z取值必须满足的一般条件:
。 |
||||||
|
恒 容 |
(4) |
1 |
3 |
0 |
b |
|
|
(5) |
0 |
0 |
|
b |
||
|
(6) |
|
2.25 |
|
b |
||
|
x、y、z取值必须满足一般条件(一个只含x、z,另一个只含y、z): ; 。 |
||||||
|
|
a与b的关系是:a
b(填>、<、=) |
|||||
13.(10分)燃料在电池中直接氧化而产生电能的装置叫燃料电池,它是一种高效低污染的新型电池。燃料电池所用燃料可以是氢气,也可以是其它燃料,如甲醇、肼等。肼分子(NH2-NH2)可以在氧气中燃烧生成氮气和水,回答下列问题:
(1)利用肼、氧气与KOH溶液组成碱性燃料电池,请写出该电池负极的电极反应式:
,并指出电解质溶液中OH-离子向 极移动。
(2)用电离方程式表示肼的水溶液呈碱性的原因 ;
(3)肼是强还原剂,与氧化剂反应时放出大量的热,如:
N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-642.2 kJ/mol
因此,肼可以作为火箭推进剂。根据以上信息,你认为是否可以通过改变反应条件,由氮气和水蒸气来制取肼 ,说明原因 。
12.双指示法可用来测定由NaOH、Na2CO3、NaHCO3中的一种或两种物质组成的混和物的含量。具体做法是:向待测液中加入酚酞,用标准盐酸滴定,当红色褪去,此时NaOH被完全中和,且Na2CO3转化为NaHCO3,消耗盐酸V1mL,然后者加甲基橙指示剂,用同一种盐酸继续滴定,当黄色变为橙色时,被转化为NaCl,消耗盐酸V2mL。
(1)判断物质的组成,请用Na2CO3、NaHCO3、NaOH填空
|
V的变化 |
V1≠0 V2=0 |
V1=0 V2≠0 |
V1>V2>0 |
V2>V1>0 |
|
试样的成分 |
|
|
|
|
(2)若盐酸的浓度为0.5mol/L,含惰性杂质的混和物的质量为1.25g,V1=30mL,V2=5mL,则各组分的百分含量是多少?
11. (12分)A、B代表不同物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。要求;相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度。
(1)写出化学式A1 ,A2 ,B1 ,B2 ;
(2)相同温度下,当A1、B1的物质的量浓度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为 ;
(3)写出0.1mol·L-1的A2溶液中离子浓度大小排序 ;
(4)B1溶液中水的电离程度小于B2溶液中水的电离程度,原因是: ;
(5)常温下,若B1、B2两溶液的pH=5,则两溶液中水电离出的氢离子的物质的量浓度之比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com