
题目列表(包括答案和解析)
19.(12分)(1) ;
(2) 。
(3) 。
(4) 、 ,
。
18.(14分)
(1) 。 (2) 。
(3) 。 (4) 。
(5)① ;② 。
(6) 。
22、已知:在氢氧化钠浓溶液中加入氧化钙,加热,制成的白色固体就是碱石灰。有两个实
验小组的同学决定通过实验探究碱石灰的组成。
(1)第一小组设计方案的流程如下:
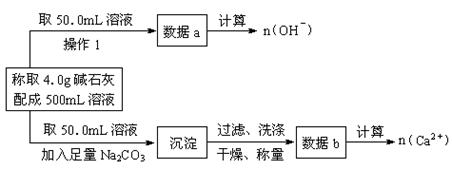
①写出n (OH-)、n (Ca2+)与n (Na+)的关系:n(Na+)= 。
②设n (Na+)=x mol、n (Ca2+)=y mol,请填写下表:
|
碱石灰的 可能组成 |
NaOH、CaO |
NaOH、CaO、 Ca (OH)2 |
NaOH、 Ca (OH)2 |
NaOH、 Ca (OH)2、H2O |
|
n
(Na+)、n (Ca2+) 的关系 |
40x+56y
= 4 |
|
|
|
(2)第二小组同学查得如下资料:Ca(OH)2在250℃时不分解、NaOH在580℃时不分解。
他们设计了如下方案并得出相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.42g,剩余固体在580℃时继续加热至恒重,固体质量又减少了0.75g。请通过计算确定该碱石灰中各成分的质量分数。

21.(14分)已知在pH为4-5的溶液中,Cu2+ 几乎不水解,而Fe3+ 几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.其实验流程图如下:
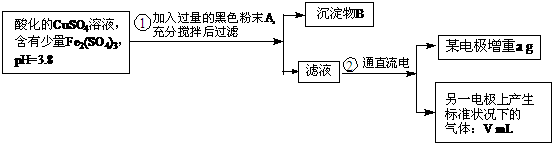
试回答下列问题:
(1)步骤①中加入A的化学式为 ,沉淀物B
是 (填化学式)。
(2)步骤②中所用部分仪器如右图所示,则A应连接直流电源的 ___极
,请写出B电极上发生反应的电极方程式: __________。
(3)下列实验操作属必要的是_____ (填字母)。
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.在空气中烘干电极,必须采用低温烘干法
E.电极在烘干称重的操作中必须按如下顺序:烘干→称重→再烘干→再称重进行至少两次
(4)电解后向溶液中加入石蕊试液,观察到的现象是 。
(5)铜的相对原子质量的计算式是___ ______________。
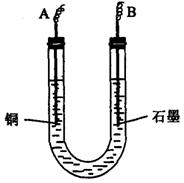
20.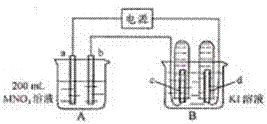 (7分)如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:
(7分)如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:
(1)a为 极,c极的电极反应式为:
。
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶
液,你能观察到的现象是
。电解进行一段时
间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为: 。
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了 mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 g·moL-1。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3溶液的物质的量浓度为 mol·L-1。
19.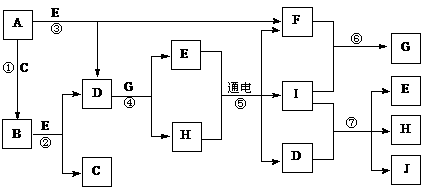 (12分)A-J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂。
(12分)A-J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂。
(1)写出E的电子式:_____________________。
(2)写出反应⑦的离子方程式:_________________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:___________________________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:__________________。________极(填“阴”或“阳”)附近溶液由无色变为红色,其原因是:__________________ _
。
18.(14分)写出下列各有机物的结构简式:
(1)当0.2mol烃A在O2中完全燃烧时生成CO2和H2O各1.2mol,催化加氢后生成2,2-二甲基丁烷。则A的结构简式为 ;
(2)某炔烃和H2充分加成后生成2,5-二甲基己烷,则该烃的结构简式为 ;
(3)某烃1mol与2molHCl完全加成,生成的氯代烷最多还可以与4molCl2发生光取代反应,则该烃的结构简式为 ;
(4)分子式为C6H12的某烯烃中所有的碳原子均在同一平面上,则该烃的结构简式为 ;
(5)某烷烃A的蒸汽的密度是相同状况下氢气密度的64倍,经测定得知该分子中共含有6个甲基。
①若A不可能是烯烃与氢气的加成产物,则A的结构简式为 ;
②若A是炔烃与氢气的加成产物,则A的结构简式为 。
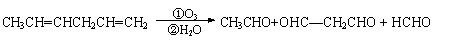 (6)已知烯烃、炔烃,经臭氧作用发生反应:
(6)已知烯烃、炔烃,经臭氧作用发生反应:

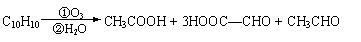 某烃分子式为C10H10,在臭氧作用下可发生如下反应:
某烃分子式为C10H10,在臭氧作用下可发生如下反应:
则C10H10的结构简式为 。
17、如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。

其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
C.若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间:Ⅰ>Ⅱ
D.平衡时Ⅰ容器的体积小于V L
第II卷(非选择题,共57分)
16.温度为25℃时,将两个铂电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,在阳极逸出a mol气体,同时有W g Na2SO4·10H2O析出,若温度不变,此时剩余溶液中的溶质的质量分数为( )
A.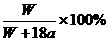 B.
B.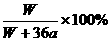 C.
C.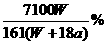 D.
D.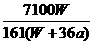 %
%
15.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是( )
 A.放电时负极反应为:Zn-2e- + 2OH- === Zn(OH)2
A.放电时负极反应为:Zn-2e- + 2OH- === Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e- + 5OH- ==== FeO42- + 4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com