
题目列表(包括答案和解析)
20. 当A、B两种气体物质的量浓度相同时,在不同温度下进行反应:A+2B=3C,
10℃时测得反应速率vB=0.2mol·l-1·S-1,50℃时测得反应速率vA=25.6mol·l-1·S-1若温度每升高10℃,该反应的反应速率增大到原来的几倍,则n约为
A 3 B 3.5 C 4 D 4.5
19. 将4
mol A气体和2 mol B气体在2L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 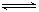 2C(g)若经2s 后测得C的浓度为0.6mol•L-1现有下列几种说法:
2C(g)若经2s 后测得C的浓度为0.6mol•L-1现有下列几种说法:
① 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1
② 用物质B 表示的反应的平均速率为0.6 mol•L-1•s-1③ 2s时物质A的转化率为70%
④ 2s时物质B的浓度为0.7 mol•L-1 其中正确的是
A. ①③ B. ①④ C. ②③ D. ③④
18.298K时2SO2 (g
)+O2 (g ) 2SO3
(g ) ,△H = -197kJ/mol 。相同温度下,向密闭容器中通入2 mol
SO2 和1 mol O2 ,达到平衡时放出热量Q1
,向另一体积相同的密闭容器中通入1mol SO2 和0.5mol O2 ,平衡时放出热量Q2 ,下列关系中正确的是
2SO3
(g ) ,△H = -197kJ/mol 。相同温度下,向密闭容器中通入2 mol
SO2 和1 mol O2 ,达到平衡时放出热量Q1
,向另一体积相同的密闭容器中通入1mol SO2 和0.5mol O2 ,平衡时放出热量Q2 ,下列关系中正确的是
A.2Q2 = Q1 B.2Q2 < Q1 C.Q1 < Q2 < Q1 /2 D.Q2 > Q1/2
16.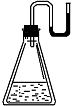 有下列物质:① NaOH固体;② 浓硫酸;③ NH4NO3晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是
有下列物质:① NaOH固体;② 浓硫酸;③ NH4NO3晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是
A.① ② ③ ④ B.① ② ④ C.② ③ ④ D.① ② ③
17 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4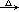 N2↑+4H2O+Cl2↑+2O2↑
N2↑+4H2O+Cl2↑+2O2↑
△H<0。下列对此反应的叙述中错误的是
A.上述反应属于分解反应 B.上述反应瞬间产生大量高温气体推动航天飞机飞行
C.反应从能量变化上说,主要是化学能转变为热能和动能
D.在反应中高氯酸铵只起氧化剂作用
15、在12g碳不完全燃烧所得气体中,CO占1/3,CO2占2/3,已知C(s)+1/2O2(g)=CO(g) △H=-110.35kJ/mol CO(g)+1/2O2(g)=CO2(g) △H=-282.57 kJ/mol,与这些碳完全燃烧相比,损失的热量是
A.172.22kJ B.36.78kJ C.73.56kJ D.94.19kJ
14、强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,向1L0.5mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓H2SO4;③稀硝酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是
A.△H1>△H2>△H3 B.△H1<△H3<△H2
C.△H1=△H3>△H2 D.△H1>△H3>△H2
13、一定温度下固定体积的容器中,X(g)+3Y(g) 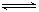 2Z(g)达化学平衡状态的标志是
2Z(g)达化学平衡状态的标志是
A. 混合气体的相对分子质量不变 B. 单位时间生成amolX,同时生成3a molY
C. 速率V(X):V(Y):V(Z)= 1:3:2 D. X、Y、Z的分子数比为1:3:2
12、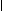
 丁苯橡胶的结构简式: n
丁苯橡胶的结构简式: n
合成该橡胶的单体是
① ②CH3-CH=CH-CH3 ③CH2=CH-CH=CH2
④ ⑤
A.①② B.④⑤ C.③⑤ D.①③
11、已知299 K时,合成氨反应 N2 (g ) + 3H2 ( g ) 2NH3 ( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3 ( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
 A、一定大于92.0 kJ B、一定等于92.0 kJ
C、一定小于92.0 kJ D、不能确定
A、一定大于92.0 kJ B、一定等于92.0 kJ
C、一定小于92.0 kJ D、不能确定
10、已知在1×105 Pa,298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
A、H2O ( g ) = H2 ( g ) + 1/2O2 ( g ) △H = +242 kJ/mol
B、2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H = -484 kJ/mol
C、H2 ( g ) + 1/2O2 ( g ) = H2O ( g ) △H = +242 kJ/mol
D、2H2 ( g ) + O2 ( g ) = 2H2O ( g ) △H = +484 kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com