
题目列表(包括答案和解析)
30.(6分)测定酸碱中和热要用稀溶液而不能用浓溶液的原因是
强酸强碱的中和热57.3 kJ/mol,弱酸、弱碱的中和反应的热量小于 57.3 kJ/mol,
其原因是 。
中和热测定中要用稍过量的碱,其目的是
2009年上学期衡阳市八中高二年级第一次月考化学答题卡
相对原子质量:H-1 O-16 C-12 N-14 S-32 Na-23 k-39 Cu-64 Fe-56 Al-27 Mg-24
0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的数值为 。
(2)氨催化氧化的化学方程式为_______________ _____,
该反应是放热反应,当温度升高时,反应的化学平衡常数K值_ _(增大、减小、无影响)。
(3)今年“两会”后,党和国家更加重视环保。工业上常用纯碱溶液来吸收硝酸厂尾气中的二氧化氮,吸收产物中有亚硝酸钠、硝酸钠和二氧化碳,该化学方程式为
____
还可以利用氢气在催化剂下把氮的氧化物还原为_____ 和水。
29.(14分)工业生产硝酸的流程图如下


(1)已知N2(g) +3H2(g)  2NH3(g) ; ΔH=-92.4kJ·mol-1。请回答:
2NH3(g) ; ΔH=-92.4kJ·mol-1。请回答:
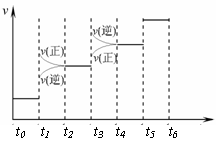 ① 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示。图中tl 时引起平衡移动的条件可能是
。 其中表示平衡混合物中NH3的含量最高的一段时间是
。
① 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示。图中tl 时引起平衡移动的条件可能是
。 其中表示平衡混合物中NH3的含量最高的一段时间是
。
②温度为T ℃时,将2a mol H2和a mol N2放入
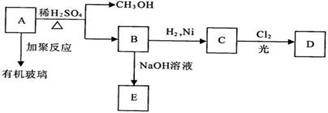
28.(6分)有机玻璃是一种重要塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化:
 请回答:
请回答:
(1) 由B转化为C的反应属于(选填序号) _____________。
① 氧化反应 ② 还原反应 ③ 加成反应 ④ 取代反应
(2) 由A生成B的化学方程式是_______。(3) 有机玻璃的结构简式是___________。
26、(4分)(1)据了解,我国兴建的三峡工程提供的水力发电功率相当于3000万kW的火力发电站。因此,三峡建设将有助于控制
A. 温室效应 B. 白色污染 C. 城市污水的任意排放D. 长江中、下游的洪涝灾害
(2)已知1 g碳粉在氧气中完全燃烧放出的热量是32.8 kJ(与1g 原煤相当),试写出相关的热化学方程式: 。
27(6分)已知CO的燃烧热为△H = -283 kJ/mol;氢气的燃烧热为△H = -286 kJ/mol; CH4的燃烧热为△H = -890 kJ/mol。
(1) 若 1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量 为 890 kJ
(2) 若x molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的取值范围是 。
(3) 若将x molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的的取值范围是: 。
25.可逆反应mA(s)+nB(g) 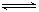 pC(g)+qD(g)。反应中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如上图,根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)。反应中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如上图,根据图中曲线分析,判断下列叙述中正确的是


A.达到平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,则平衡向逆反应方向移动
C.平衡后,增大A的量,有利于平衡正向移动
D.化学方程式中一定有m+n<p+q
24.
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生下列反应:2SO2(g)+O2(g)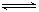 2SO3(g),并达到平衡。在这过程中甲容器压强保持不变,乙容器保持体积不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3(g),并达到平衡。在这过程中甲容器压强保持不变,乙容器保持体积不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A. 等于p% B. 大于p% C. 小于p% D. 无法判断
23. 某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g) 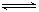 cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
A. 平衡正移 B. (a+b)>(c+d) C. Z的体积分数变小 D. X的转化率变大
22. 有一处于平衡状态的反应:X(s)+3Y(g) 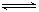 2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤ B.②③⑤ C.②③⑥ D.②④⑥
21. 在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)  2C(g),可以判断达到化学平衡状态的是
2C(g),可以判断达到化学平衡状态的是
A. 体系压强不变 B. 单位时间消耗n molA,同时生成2nmolC
C. A的转化率不变 D. 容器内气体密度不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com