
题目列表(包括答案和解析)
5.油脂水解的产物是:
A.酸和甘油 B.氨基酸 C.葡萄糖 D.肥皂
4.垃圾资源化的方法是:
A.填埋法 B.焚烧法 C.堆肥法 D.分类回收法
3.下面不是污水化学处理方法的是:
A.过滤法 B.混凝法 C.中和法 D.沉淀法
2.关于合理饮食有利于健康的下列说法正确的是:
A.没有水就没有生命 B.调味剂和营养剂加得越多越好
C.养成良好的饮食习惯,多吃蔬菜、水果等碱性食物
D.饮用水越纯净越好
1.维生素C具有的性质是:
A.难溶于水 B.易分解
C.还原性 D.氧化性
25、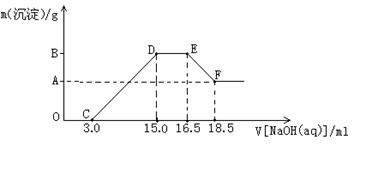 (12分)硝酸跟金属反应时,随着硝酸的浓度下降和金属活动性的增大,产物中氮元素的化合价会逐渐下降.现有一定量铁粉和铝粉组成的混合物跟100ml稀硝酸充分反应,反应过程中无任何气体放出,在反应结束后的澄清溶液中,逐渐加入4.00mol/L的氢氧化钠溶液,加入氢氧化钠溶液的体积与产生沉淀的质量如图所示:
(12分)硝酸跟金属反应时,随着硝酸的浓度下降和金属活动性的增大,产物中氮元素的化合价会逐渐下降.现有一定量铁粉和铝粉组成的混合物跟100ml稀硝酸充分反应,反应过程中无任何气体放出,在反应结束后的澄清溶液中,逐渐加入4.00mol/L的氢氧化钠溶液,加入氢氧化钠溶液的体积与产生沉淀的质量如图所示:
请回答:
(1)D点时溶质为 (填化学式)
图形中DE段的离子方程式为:
EF段的离子方程式为:______________________________________
(2)求纵坐标中A点的数值和原稀硝酸的浓度
24、(10分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应 ,负极反应 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,设计除去CuCI2溶液中Fe3+和Fe2+的三个实验步骤
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式 、
证明劣质不锈钢腐蚀的实验现象: 。
23.(10分)A-J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,J是一种红褐色沉淀,H的焰色反应呈黄色。
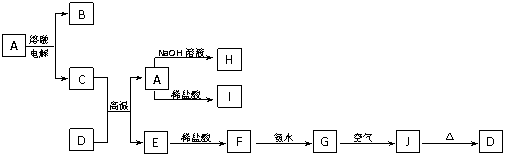
请回答下列问题:
(1)A物质的化学式为_________,E在周期表中的位置____________。
(2)G→J的化学方程式为___________________________________。
(3)C+D→A+E的化学方程式为______________________________。
(4)C与氢氧化钠溶液反应的离子方程式为________________________,所得溶液中加入过量盐酸后存在的阳离子化学式为________________。
22、(10分)
(1)已知:25℃时,某强酸溶液 pH=a,某强碱溶液pH=b。若a+b=14,两者等体积混合后,溶液的pH= ___ ,此时若溶液中阳离子浓度大于阴离子浓度,其原因可能是_________;若强酸强碱按体积比为1:10混合后溶液显中性,则a+b=_________
(2) 常温下,如果取pH=4的酸H3B溶液与pH=10的 溶液等体积混合后溶液呈酸性,生成盐的化学式为_________;
溶液等体积混合后溶液呈酸性,生成盐的化学式为_________;
(3)常温下,在pH为3的FeCl3溶液和pH为3的盐酸中由水电离出来的 的浓度
的浓度
分别为:C1和C2,则C1 :C2为
(4)将4.48 L(标准状况下)CO2通入100 mL3 mol/LNaOH的水溶液后,溶液中离子浓度由大到小的顺序为 。
19.气态烃组成的混和气体,对氢气的相对密度为13,取此混和气体4.48L(标准状况下)通入足量溴水,溴水增重2.8g,则此混和气体的组成是 A、CH4与C3H6 B、C2H4与C3H6 C、C2H4与CH4 D、CH4与C4H8
20将3.5gFe、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体V L(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量的氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗净、干燥后称量质量为8.6g。则收集到的气体体积V值可为 A.1.12 B.5.34 C.7.26 D.8.23
Ⅱ卷 (非选择题 52分)
21题(10分)
(1)下面五种物质的沸点由高到低的顺序正确的是 (填序号)
①正戊烷 ②正庚烷 ③2-甲基己烷④3,3-二甲基戊烷 ⑤异丁烷
(2)0.1mol某烃在足量的氧气中完全燃烧,生成水10.8g和二氧化碳26.4g,则该烃的分子式为_______;若该烃分子中共面碳原子数最多,该烃名称为
若该烃不能使溴水退色,且一氯代物只有一种,其结构简式为
;若该烃能与氯化氢发生加成反应,但加成产物只有一种的烃有 种,若该烃能使溴水褪色该烃在催化剂作用下,与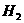 发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为___________,写出该烃在催化剂作用下发生加聚反应的化学方程式:__________
发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为___________,写出该烃在催化剂作用下发生加聚反应的化学方程式:__________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com