
题目列表(包括答案和解析)
8.下列实验现象描述正确的是
A.氯化氢与氨气相遇,有大量的白雾生成
B.用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色
C.氯化亚铁溶液与无色的KSCN溶液混合,溶液呈红色
D.SO2通入品红溶液,红色褪去,再加热,红色不再出现
6.在强酸性溶液中,可以大量共存的离子是 A.K+、Na+、SO42-、CO32- B.NH4+、Mg2+、SO42-、Cl- C.Na+、K+、HCO3-、Cl- D.K+、Na+、AlO2-、NO3- 7.铝制餐具不宜经常用热碱水洗涤的原因是
A.铝在常温下性质稳定 B.铝有还原性
C.铝和氧化铝都可与碱溶液反应 D.铝表面的氧化膜受热会分解
5.能够将溶液和胶体区分开的方法是
A.过滤 B.观察颜色、状态 C.利用丁达尔效应 D.闻气味
3.下列有关环境问题都是由化学物质引起的,在下列组合中对应的化合物不正确的是 A.温室效应:二氧化碳 B.光化学烟雾:二氧化氮 C.酸雨:二氧化碳 D.臭氧层破坏:氟氯烃 4.能够用于鉴别SO2和CO2的溶液是
A. 石蕊试液 B. 品红溶液 C. 澄清石灰水 D. 氯化钡溶液
2.下列有机物在空气中燃烧,产生明亮并带有浓烟火焰的物质是
A.CH4 B.CH2==CH2 C.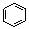 D.CH3CH2OH
D.CH3CH2OH
1.分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“Na2SiO3”的分类不正确的是
A.离子化合物 B.电解质 C.钠盐 D.碱性氧化物
26.(10分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热后,收集到0.08 mol气体。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g.。
根据上述实验,回答以下问题:
(1) 由第一份进行的实验推断该混合物是否一定含有Cl-
(2) 由第二份进行的实验得知混合物中应含有 离子,其物质的量浓度为
(3) 由第三份进行的实验可知12.54g沉淀的成分为
请计算形成该沉淀的原混合物中各离子的物质的量。(要求计算过程)
(4) 综合上述实验,你认为以下结论正确的是
A. 该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K+) ≥0.04mol
B. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl-
C. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl-
D. 该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl-
25.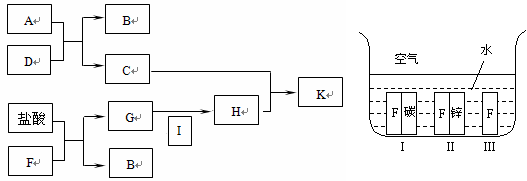 (6分)下方左图中A~K均为中学化学中常见的物质,其中A和F是金属单质,D是最常见的溶剂。I为黄绿色气体,C的焰色反应呈黄色,K是红褐色固体。
(6分)下方左图中A~K均为中学化学中常见的物质,其中A和F是金属单质,D是最常见的溶剂。I为黄绿色气体,C的焰色反应呈黄色,K是红褐色固体。
(1)A的元素在周期表中位于第 周期 族 。
(2)A+D→B+C的离子方程式为 。
G+I→H的离子方程式为 。
(3)实验室常用KSCN溶液检验H中的金属离子,现象是 。
(4)如上方右图所示,F处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,该金属被腐蚀的速率由快到慢的顺序是(填序号)_______________。
24.(15分)
A.(Ⅰ)我国采用食盐中加入碘酸钾(KIO3)的方法防止缺碘引起的疾病。
⑴在人体中,碘是属于 (选填“常量”或“微量”)元素;缺碘引起的疾病有 。
⑵已知在酸性溶液中IO3-可和I-发生反应:IO3-+5I-+6H+=3I2+3H2O,萃取碘水中的碘时,可选用的试剂是 ;利用上述反应,检验食盐中是否有碘酸钾必须使用的物质是____________(可供选用的有:①稀硝酸,②蓝色石蕊试纸,③碘化钾淀粉试纸,④淀粉,⑤食糖,⑥食用白醋溶液)。
⑶已知碘酸钾受热易分解,在用碘酸钾加碘盐进行烹饪时应注意 。
(Ⅱ)蛋白质是生命的基础,没有蛋白质就没有生命。请回答下列问题:
⑷蛋白质分子中主要含有____________________等三种元素。
⑸蛋白质是人体必需的营养物质之一,下列各类食物中,蛋白质含量最丰富的是 。

A. B. C. D.
 ⑹ 蛋白质在一定条件下能发生变性,从而失去生理活性。万一误服硫酸铜溶液,此时应立即作怎样的处理?_______________________。
⑹ 蛋白质在一定条件下能发生变性,从而失去生理活性。万一误服硫酸铜溶液,此时应立即作怎样的处理?_______________________。
⑺一种二肽的结构简式如右图。合成这种二肽的氨基酸的结构简式是 、 。
(Ⅲ)自然环境与人们的生活息息相关。寻找源头治理环境是当今化学工作者面临的重要任务。
⑻甲乙两工厂排放的污水中含有下列六种离子中的三种(Na+、Ag+、Cu2+、OH-、Cl-、NO3-),将两厂污水混合排放可减少污染,已知乙厂污水呈碱性,则乙厂污水所含的其他两种离子是 、 。
若两厂污水混合重金属离子能完全除去,混合后的水直接排放到河中会引起 。
⑼向煤中加入适量石灰石,可大大减少燃烧产物中SO2的量,并有硫酸钙生成,写出上述反应的总反应式是____________________________________。
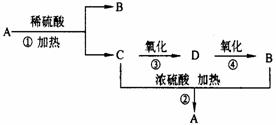 B. (Ⅰ)(8分)化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
B. (Ⅰ)(8分)化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
(1)A的名称是 。
(2)B的结构简式是 。
(3)D中含有的官能团(填名称) 。
(4)写出B和C生成A的化学方程 式 。
(Ⅱ)(7分)甲苯和溴乙烷混合物可通过如下流程进行分离。
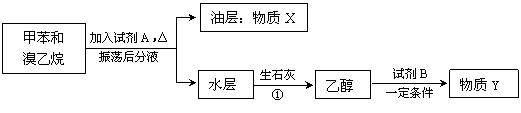
请填写下列空白:
⑴ 试剂A的名称为 ;X的结构简式为 ;
⑵ 操作①是 ;
⑶ 写出在甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式: 。
第Ⅱ卷(非选择题 共31分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com