
题目列表(包括答案和解析)
8.下列溶液混合后,pH 值最大的是( )
A.0.1mol/LH2SO4与0.2mol/L 氨水各50mL
B.0.1mol/LCH3COOH与0.1mol/LNaOH 溶液各50mL
C.pH = 1的CH3COOH与pH = 13的 NaOH 溶液各50mL
D.pH = 1的盐酸与 pH = 13的 NaOH 溶液各50mL
7.将 0.06mol·L-1H2SO4溶液与0.10mol·L-1NaOH 溶液等体积混合后,所得溶液的pH 为( )
A.1.7 B.2.0 C.12.0 D.12.3
6.将一块去掉氧化膜的锌片放入100 mL pH为1的盐酸中,2 min后溶液的pH变为2,则产生H2的速率可表示为(设溶液体积不变) ( )
A. 0.0225 mol / (L·min) B. 0.05 mol / (L·min)
C. 0.045 mol / (L·min) D. 0.01 mol / (L·min)
5.某溶液100 mL,室温时测得其pH等于1,下列叙述中不正确的是 ( )
A. 该溶液c(H+)≥0.1 mol / L
B. 把该溶液稀释成1 L后,pH ≥ 2
C. 把该溶液稀释成1 L后,pH ≤ 2
D. 中和此溶液需0.1mol / L的NaOH体积≥100mL
4.甲乙两种溶液,已知甲溶液的pH是乙溶液pH的2倍,则甲溶液的c(H+)与乙溶液的c(H+)关系是 ( D )
A.1/2倍 B.1/100倍 C. 100倍 D. 无法确定
3.室温时,0.01mol·L-1某一元弱酸的电离度为 1% ,则下列说法正确的是 ( )
A.上述弱酸溶液的 pH = 4
B.加入等体积 0.01mol·L-1NaOH 溶液后,所得溶液的 pH = 7
C.加入等体积 0.01mol·L-1NaOH 溶液后,所得溶液的 pH > 7
D .加入等体积 0.01mol·L-1NaOH 溶液后,所得溶液的 pH < 7
2.若pH = 3的酸溶液和pH = 11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
A.生成了一种强酸弱碱性盐 B.弱酸溶液和强碱溶液反应
C.弱酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
1.用 0.1mol·L-1NaOH 溶液滴定 0.1mol·L-1盐酸,如达到滴定的终点时不慎多加了 1滴 NaOH 溶液(1滴溶液的体积约为 0.05mL),继续加水至 50mL,所得溶液的 pH 是 ( )
A.4 B.7.2 C.10 D.11.3
4、溶液稀释时pH的计算
①对于强酸溶液,c(H+)每稀释10n倍,pH增大n个单位,但不突破7。
②对于强碱溶液,c(OH-)每稀释10n倍,pH减小n个单位,但不突破7。
③对于pH相同的强酸与弱酸(或强碱与弱碱)稀释相同倍数时,pH变化程度不同,其结果是强酸(或强碱)pH变化大,而弱酸(或弱碱)pH变化小。
练习题
3、强酸强碱混合,其中一种物质过量的pH的计算
①酸过量时,先求c混(H+),再求pH,c混(H+)=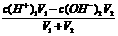
②碱过量,先算c混(OH-),再算c混(H+),最后算pH,c混(OH-)=
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com