
题目列表(包括答案和解析)
18、下表是某温度下测得某酸溶液的一些数据,由表中的数据填空:
|
溶液的物质的量浓度/mol·L-1 |
电离度/% |
H+的物质的量浓度/mol·L-1 |
pH |
|
0.1 |
2α |
c1 |
x |
|
c |
α |
2c1 |
3 |
则 c= ;α = ;c1= ;x=
17.某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH为11,则该温度下水的KW= 。在此温度下,将 pH = a的 NaOH 溶液 VaL 与 pH = b的 H2SO4溶液 VbL 混合,
(1)若所得混合液为中性,且 a= 12,b= 2,则 Va∶Vb= ;
(2)若所得混合液为中性,且 a+ b= 12,则 Va∶Vb= ;
(3)若所得混合液的 pH = 10,且 a= 12,b= 2,则 Va∶Vb= 。
16、某温度下的溶液中,c(H+)= 10xmol/L,c(OH-)= 10ymol/L。x与 y的关系如右图所示:
(1)求该温度下,中性溶液的 pH。
(2)求该温度下 0.01mo/LNaOH 溶液的 pH。
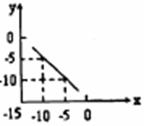 (3)该温度下,pH
= a的醋酸溶液与 pH = b 的 NaOH 溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度。
(3)该温度下,pH
= a的醋酸溶液与 pH = b 的 NaOH 溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度。
选做题
15.已知浓度均为0.1mol/L的8种溶液:①HNO3 ②H2SO4 ③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl其溶液pH由小到大的顺序是______________________。
14.25℃时向纯水中加入NaOH使其浓度为0.1 mol / L,则此时溶液中水电离出的c(OH-)是 mol / L。
13.在200 mL氢氧化钡溶液中含有1×10-3 mol的钡离子,溶液的pH为____。将此溶液与pH=3的盐酸混合,使其混合溶液的pH=7,应取氢氧化钡溶液和盐酸的体积之比是 _ 。
12.将 pH = 1的盐酸平均分成两份,一份加适量的水,另一份加与该盐酸物质的量浓度相同的适量氢氧化钠溶液后,pH 都升高了 1,则加入水与氢氧化钠溶液的体积比是( )
A.9 B.10 C.11 D.12
11.在 pH = 9的氢氧化钠和 pH = 9 的醋酸钠的两种溶液中,假设由水电离出的氢氧根离子的物质的量浓度分别为 Amol·L-1和 Bmol·L-1,则 A 和 B 的关系是( )
A.A = 1×10-4B B.B = 1×10-4A C.A > B D.A = B
10.将pH=5的稀硫酸溶液稀释500 倍,稀释后溶液中c(SO42-)与c(H+)之比约为( )
A.1∶1 B.1∶2 C.1∶10 D.10∶1
9.为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG = lgc(H+)/c(OH-),则下列叙述正确的是( )
A.中性溶液的 AG = 0 B.酸性溶液的AG < 0
C.常温下0.1mol/LNaOH溶液的AG = 12 D .常温下0.1mol/L盐酸溶液的AG = 12
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com