
题目列表(包括答案和解析)
(二)水解规律 简述为:
1.正盐溶液 ①强酸弱碱盐呈 。②强碱弱酸盐呈 。
③强酸强碱盐呈 。④弱酸弱碱盐不一定
2.酸式盐
①若只有电离而无水解,则呈酸性(如NaHSO4)
②若既有电离又有水解,取决于两者相对大小 电离程度>水解程度,呈
电离程度<水解程度,呈
③常见酸式盐溶液的酸碱性 碱性:NaHCO3、NaHS、Na2HPO4、NaHS.
酸性:NaHSO3、NaH2PO4、NaHSO4
(一) 盐的水解实质: 。
1.甲酸和乙酸都是弱酸,当它们的浓度均为0.10mol/L时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知
A.a的浓度必小于乙酸的浓度 B.a的浓度必大于乙酸的浓度
C.b的浓度必小于乙酸的浓度 D.b的浓度必大于乙酸的浓度
2.用水稀释0.1 mol·L-1氨水时,溶液中随着水量的增加而减小的是
A.c(OH-)/c(NH3·H2O) B.c(NH3·H2O)/c(OH-)
C.c(H+)和c(OH-)的乘积 D.OH-的物质的量
3. 某二元弱酸(H2A)溶液,按下式发生一级和二级电离:
H2A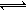 H++HA- HA-
H++HA- HA-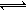 H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>>α(HA-),设有下列四种溶液:
A.0.01mol·L-1的H2A 溶液
B.0.01mol·L-1的NaHA 溶液
C.0.02mol·L-1的HCl溶液与0.04mol·L-1的NaHA溶液等体积混合液
D.0.02mol·L-1的NaOH溶液与0.02mol·L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(1)c(H+)最大的是 ,最小的是
(2)c(H2A)最大的是 ,最小的是
(3)c(A2-)最大的是 ,最小的是
盐类的水解
重点回顾
15.对比同体积、同浓度的盐酸和醋酸,c(H+)前者 后者,与碱完全中和时,消耗NaOH的物质的量是前者 后者,与足量的Zn反应产生H2的速率是前者 后者,产生H2的量是前者 后者。(填“>”、“<”或“=”)
14.在稀氨水中存在平衡:NH3+H2O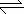 NH
NH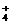 +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH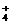 、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。 (1)通适量HCl气体时,c(NH3)
,c(H+)
。
、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。 (1)通适量HCl气体时,c(NH3)
,c(H+)
。
(2)加入少量NaOH固体时,c(NH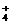 )
,c(OH-) 。
)
,c(OH-) 。
(3)加入NH4Cl晶体时,c(NH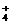 )
,c(OH-)
。
)
,c(OH-)
。
13.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答:
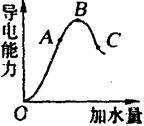 (1)“O”点导电能力为“0”的理由是_______________________。
(1)“O”点导电能力为“0”的理由是_______________________。
(2)A、B、C三点pH值由大到小的顺序是_______________________。
(3)A、B、C三点电离程度最大的是____________________
12.在一定温度下,有a盐酸,b硫酸,c醋酸,三种酸:
(1)当三种酸物质的量浓度相等时,c(H+)由大到小的顺序是
(2)若三者c(H+)相同,物质的量浓度由大到小的顺序是
(3)将c(H+)相同的三种酸均加水稀释至原来的100倍,c(H+)由大到小的顺序是
10. 在含有酚酞的0.1 mol/L氨水中加入少量的NH4Cl晶体,则溶液颜色
A.变蓝色 B.变深 C.变浅 D.不变
11 将0.1mol·L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起
A.溶液的pH增加 B.促进CH3COOH的电离
C.溶液的导电能力减弱 D.溶液中c(OH-)减少
9. 在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:
CH3COOH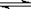 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
8. 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是
A.通入二氧化碳气体 B.加入氢氧化钠固体
C.通入氯化氢气体 D.加入饱和石灰水溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com