
题目列表(包括答案和解析)
5、已知某反应的焓变小于零,则下列叙述正确的是( )
A.该反应一定是放热反应
B.该反应一定是吸热反应
C.该反应反应物的总能量一定大于产物的总能量
D.该反应产物的总能量一定大于反应物的总能量
4、阿伏加德罗常数的数值记为NA,则关于反应:
 C2H2(g)+
C2H2(g)+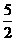 O2(g) 2CO2(g)+H2O(l)
O2(g) 2CO2(g)+H2O(l)
△H=-1300kJ·mol-1
下列说法中,正确的是( )
A.有10NA个电子转移时,吸收1300kJ的能量
B.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
C.有NA个水分子生成且为液体时,吸收1300kJ的能量
D.有2NA个碳氧双键生成时,放出1300kJ的能量
3、下列反应中生成物的总能量大于反应物总能量的是( )
A.氢气在氧气中燃烧 B.铁丝在氧气中燃烧
C.硫在氧气中燃烧 D.焦炭在高温下与水蒸气反应
2、 某短跑运动员体重70kg,起跑时以1/7秒冲出1m远,消耗的能量为6860J,其能量全部由消耗体内葡萄糖提供,热化学方程式为C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(1);
某短跑运动员体重70kg,起跑时以1/7秒冲出1m远,消耗的能量为6860J,其能量全部由消耗体内葡萄糖提供,热化学方程式为C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(1);
△H=-2804kJ·mol-1,则所消耗葡萄糖的质量为( )
A.0.22g B.0.55g C.0.44g D.0.66g
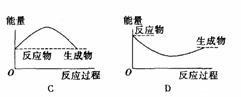
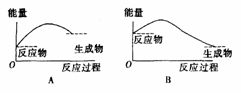
1、下列各图中,表示正反应是吸热反应的是( )
2.热化学方程式书写的注意事项
(1)要在物质的 后面用括号注明物质的 。一般用英文字母g、l和s分别表示物质的
态、 态、 态。水溶液中的溶质则用 表示。
(2)在△H后要注明 ,因为在不同 下进行同一反应,其反应 是不同的。在溶液中的反应应注明 以及 的浓度。
(3)△H的单位是 或 。
|
[基础训练]
1.在热化学中,将一个化学反应的 变化和反应的 变同时表示出来的化学方程式称为热化学方程式。因此,热化学方程式既遵循 守恒,又遵循 守恒。
2.焓变
(1)定义: ,称为化学反应的焓变。
(2)表达式: 。
(3)焓变与反应热的关系:如果化学反应过程中体系的压强不变即发生等压反应,而且没有电能、光能等其他形式能量转化,则反应热等于反应焓变即Qp=△H(Qp为等压条件下该化学反应的反应热)。从上面的关系式可以看出:△H>0时,产物的总焓 反应物的总焓,反应是 能量的,为 反应;△H<0时,产物的总焓 反应物的总焓,反应是
能量的,为 反应。
(4)计算方法:
对于一个化学反应,无论是 完成还是分 完成,其反应 是一样的,这一规律称为盖斯定律。
1.焓
(1)含义: ,科学上用焓这一物理量来描述物质的这一固有性质。
(2)大小影响因素:对于一定量的纯物质,在一定的状态(温度、压强)下,焓有确定的数值,它的数值的大小与物质具有的 有关。
①在同样条件下,物质所具有的能量不同,焓的数值不同;
②同一物质所处的外界条件(温度、压强)不同,焓的数值也不同;
③焓的数值大小与物质的量有关,在相同条件下,当物质的量增大l倍时,焙的数值也增大1倍。
2.反应热的测定
(1)测定反应热的仪器称为 ,它由 、 两个筒组成, 筒的外壁覆盖着
层。测定时,将反应物加入 筒并使之迅速混合,测量反应前后溶液的 ,并计算出反应前后溶液 的变化值。
(2)计算:用C表示体系的 ,其单位是 ;用T1和T2分别表示反应前后体系的 ,则反应热的计算公式为 。单位: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com