
题目列表(包括答案和解析)
13、下列叙述正确的是( )
①原电池是把化学能转化为电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③不能自发进行的氧化还原反应,通过原电池的装置均可实现
④碳棒不能用来做原电池的正极
 ⑤反应Cu+2Ag+ 2Ag+Cu2+,能以原电池的形式来实现
⑤反应Cu+2Ag+ 2Ag+Cu2+,能以原电池的形式来实现
A.①⑤ B.①④⑤ C.②③④ D.②⑤
12、
 有A、B、D、E四种金属,当A、B组成原电池时,电子流动方向为A→B;当A、D组成原电池时,A为正极;B与E做电极构成原电池时,电极反应为:E2++2e- E;B B2++2e-,则A、B、D、E金属性由强到弱的顺序是( )
有A、B、D、E四种金属,当A、B组成原电池时,电子流动方向为A→B;当A、D组成原电池时,A为正极;B与E做电极构成原电池时,电极反应为:E2++2e- E;B B2++2e-,则A、B、D、E金属性由强到弱的顺序是( )
A.A>B>E>D B.A>B>D>E C.D>E>A>B D.D>A>B>E
11、下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速度加快
10、用质量均为100g的铜作电极,电解硝酸银溶液,电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
A.阳极100g,阴极128g B.阳极93.6g,阴极121.6g
C.阳极91.0g,阴极119.0g D.阳极86.0g,阴极114.0g
9、1LK2SO4和CuSO4混合溶液中c(SO )=2mol/L,用石墨作电极电解此溶液,通电一段时间后,两极均收集到(标准状况下)22.4L气体,则原溶液中K+浓度为( )
)=2mol/L,用石墨作电极电解此溶液,通电一段时间后,两极均收集到(标准状况下)22.4L气体,则原溶液中K+浓度为( )
A.0.5mol/L B.1mol/L C.1.5mol/L D.2mol/L
8、有含少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了m g,则( )
A.电解液质量增加m g B.阴极质量增加a g ,a>m
C.阴极质量增加m g D.阴极质量增加b g ,b<m
7、在铁制品上镀一定厚度的锌层,以下设计方案设计正确的是( )
A.锌作阳极,镀件作阴极,溶液中含有锌离子
B.铂作阴极,镀件作阳极,溶液中含有锌离子
C.铁作阳极,镀件作阴极,溶液中含有亚铁离子
|
6、下列过程需要通电后才能进行的是( )
①电离②电解③电镀④电泳⑤电化腐蚀
A.①②③ B.②③④ C.②④⑤ D.①②③④⑤
5、下列有关热化学方程式的叙述中,正确的是( )
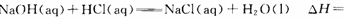 A.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为
+57.4 kJ·mol-1
A.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为
+57.4 kJ·mol-1
 B.已知C(石墨,s)
C(金刚石,s)
B.已知C(石墨,s)
C(金刚石,s)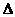 H>0,则金刚石比石墨稳定
H>0,则金刚石比石墨稳定
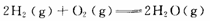 C.已知
C.已知
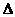 H=-483.6kJ·mol-1,则H2的燃烧热为241.8 kJ·mol-1
H=-483.6kJ·mol-1,则H2的燃烧热为241.8 kJ·mol-1
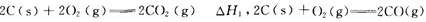 D.已知
D.已知
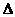 H2,则
H2,则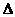 H1<
H1<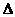 H2
H2
4、
 对于Zn(s)+H2SO4(l) ZnSO4(l)+H2(g)
对于Zn(s)+H2SO4(l) ZnSO4(l)+H2(g)
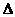 H<0的化学反应,下列说法一定正确的是( )
H<0的化学反应,下列说法一定正确的是( )
A.反应过程中能量关系可用右图表示
B.1 mol锌所含的能量高于1 molH2所含的能量
C.若将该反应设计成原电池,锌为正极
D.若将其设计为原电池,当有32.5g锌溶解时,正
极放出气体一定为11.2L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com