
题目列表(包括答案和解析)
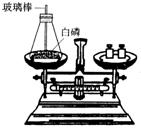
6.如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验。
(1)写出白磷燃烧的化学方程式_____________________________。
(2)白磷在锥形瓶中燃烧时,常常导致瓶塞被冲开,实验失败。导致瓶塞被冲开的原因是_____________________________________。
(3)为了防止瓶塞被冲开,你能将实验作如何的改进?________________。
(4)实验时,用加热后的玻璃棒点燃白磷,你还能找出其他方法点燃瓶内的白磷吗?________________________________________________________。
5.早在17世纪,质量守恒定律被发现之前,英国化学家波义耳曾做过一个实验:在密闭的玻璃容器中燃烧金属,得到了金属灰,然后称量金属灰的质量,发现比原金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
4.在反应中,当1.6g X与Y完全反应后,生成R的质量为4.4g,且反应后生成的R和M的质量之比为11:9,则在此反应中Y和M的质量比是( )
A. 23:9 B. 16:9 C. 32:9 D. 46:9
3.如右图所示,二分子的甲反应生成二分子的乙与一分子的丙,已知甲、乙、丙三者为不
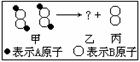 同的纯净物。则从图示中获得的下列信息中错误的是( )
同的纯净物。则从图示中获得的下列信息中错误的是( )
A.分子的种类在化学反应中发生了改变
B.该反应的反应类型为分解反应
C.化学变化中原子的种类没有改变 D.乙分子中含有4个A原子、2个B原子
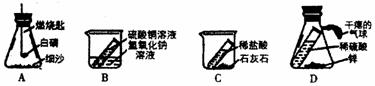
2.下列装置不能用做证明质量守恒定律实验的是( )
1.宣传科学知识,揭露伪科学是我们的义务,下列说法中,属于伪科学的是( )
A.氢气可用作高能燃料 B.以石油为原料可蒸馏出汽油等产品
C.农业上主要施用含氨、磷、钾元素的肥料 D.“气功”能使铜变成金
2.对质量守恒定律的适用范围含糊不清:①必须在化学反应中,如:100g酒精和100g水混合形成200g酒精溶液,并不能用质量守恒定律解释;②在利用质量守恒定律时,一定要注意是参加反应的总质量和生成物的总质量才相等。如:酒精燃烧后,质量逐渐减少,用质量守恒定律来解释的话,参加反应的酒精和氧气的质量总和应该与生成的二氧化碳及水的总质量相等,而二氧化碳和水散失在空气中,无法称得质量,所以质量减少。而铁钉生锈后质量会增加,则是因为参加反应的铁和氧气的质量总和等于生成的铁锈的质量,当然铁锈的质量就会大于原先金属铁的质量。
[基础演练]
1.质量守恒定律成立的原因理解的不够透彻:①根据化学反应的本质,原子的重组,即参加反应的各原子的种类、数目不变,质量也基本不变;②在宏观上,元素的种类和质量也不变。如例2。
5.给出某具体化学反应方程式,能说出其所代表的涵义或信息,如例5。
[典例精析]
例1:(四川省中考)为了验证质量守恒定律。甲、乙、丙三位同学各做了一个实验。
(1)甲同学用实验测定的数据有:木炭和坩埚的总质量mg;其燃烧后灰烬和坩埚的总质量为ng。 m和n的关系为:m n(填“<”或“>”或“=”)。
(2)乙同学用实验测定的数据有:光亮的铁钉的质量为xg;其生锈后的质量为了yg。 x和y的关系为:x y(填“<”或“>”或“=”)。
(3)丙同学实验测定的数据有:锌、硫酸铜溶液和烧杯的总质量为ag;其反应后的混合物和烧杯的总质量为bg。a与b的关系为:a b(填“<”或“>”或“=”)。
(4)通过对三个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,应 ,才能判定参加化学反应的反应物总质量和生成物总质量是否相等。
解析 题中的三个实验,分别是有气体生成、有气体参加的反应及溶液中既无气体参加也无气体生成的反应。实验数据表面上所得出的结论截然不同,实验(1)仅测定反应后灰烬和坩埚的总质量;实验(2)测定的是反应后的混合物和烧杯的总质量。它们都忽略了气体的质量。实验(3)中没有气体参加反应,也没有气体生成,其数据真实地体现了反应前后物质的质量关系。
答案:(1)> (2)< (3)= (4)在密闭的体系中实验
例2:(大连市中考)化学反应前后,下列各项中,肯定没有变化的是:( )
①原子数目;②分子数目;③元素种类;④物质的总质量; ⑤物质的种类;⑥原子的种类
A.①③④⑤⑥ B.①③④⑥ C.①②⑥ D.①③⑤
解析 可从质量守恒定律和化学反应实质去考虑问题:参加化学反应的各物质的质量总和等于生成的各物质的质量总和;在化学反应中,分子分解成原子,原子重新组合成新的分子,原子的种类、数目、质量均不发生变化。
答案:B
 例3:(泉州市中考)绿色植物进行光合作用的过程如下:
例3:(泉州市中考)绿色植物进行光合作用的过程如下:
则关于淀粉组成的说法中正确的是( )
A.只含镁、氢元素 B.含有碳、氧、氢三种元素
C.含有碳氢元素、可能含有氧元素 D.无法确定
解析 根据质量守恒定律,化学反应前原子种类、原子个数、原子质量都不改变,由光合作用的反应物是二氧化碳和水,可知生成物淀粉中一定含有碳、氢元素,又由于生成了氧气,二氧化碳和水中的氧元素是否全部转化为氧气不能确定,所以淀粉中可能含有氧元素。
答案:C
例4:(宜昌市中考)小新用在空气中燃烧镁带的实验来探究质量守恒定律:
(1)镁带燃烧的化学方程式为 。
(2)完全燃烧后,称量留下固体的质量比反应前镁带的质量还轻,联系实验过程分析,其原因可能有: ; ;……
解析 此题属于探究型开放试题。镁在空气中燃烧,有氧气参加反应,生成物氧化镁又是固体,按理来说生成的氧化镁的质量应大于参加反应镁的质量,为什么氧化镁的质量反而小了呢?肯定实验中造成了一部分氧化镁损失掉了,这就要从实验过程中的实际情况来分析,实验中有白烟冒出,反应后坩埚钳上留有白色粉末等。
答案:(1)2Mg+O2 2MgO(2)镁带燃烧时有一缕白烟(氧化镁)向空气中扩散,造成氧化镁的损失,镁带燃烧时夹镁带的坩埚钳上有一层白色粉末,此粉末为氧化镁,也造成氧化镁的损失,称量误差;……(其他合理答案均可)
2MgO(2)镁带燃烧时有一缕白烟(氧化镁)向空气中扩散,造成氧化镁的损失,镁带燃烧时夹镁带的坩埚钳上有一层白色粉末,此粉末为氧化镁,也造成氧化镁的损失,称量误差;……(其他合理答案均可)
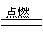
例5:(南京市中考)右下图四位同学正在讨论某一个化学方程式表示的意义,他们所描述的化学方程式是( )

A.S+O2 SO2

B.2CO+O2 2CO2

C.2H2 + O2 2H2O

D.CH4 + 2O2 CO2+2H2O
解析 本题利用图示展示了化学方程式表示的意义,根据各物质的分子个数比为2:1:2排除A、D,再根据各物质的质量比为1∶8∶9,排除B。
答案:C
[常见误区]
4.能用质量守恒定律解释日常生活中的现象例4。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com