
题目列表(包括答案和解析)
7.分别向含有下列离子的溶液中加入NaOH固体(溶液体积不变),能引起离子浓度减少的是 ( )
A.Cl- B.OH- C.[Al(OH)4]- D.HCO3-
6.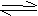 一定条件下的密闭容器中,进行如下反应NO(g)+CO(g)
一定条件下的密闭容器中,进行如下反应NO(g)+CO(g) 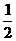 N2(g)+CO2(g),△H﹤0,达到平衡后,为提高该反应的反应速率和NO的转化率,采取的措施正确的是 ( )
N2(g)+CO2(g),△H﹤0,达到平衡后,为提高该反应的反应速率和NO的转化率,采取的措施正确的是 ( )
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
5.下列叙述正确的是 ( )
A.强弱电解质的根本区别在于电离时是否存在电离平衡
B.所有的离子化合物都是强电解质,所有的共价化合物都是弱电解质
C.弱电解质的水溶液中只有离子,没有分子
D.强电解质融化状态下都能导电
4.已知:H2C2O4是二元弱酸;KHC2O4溶液呈酸性。在0.1mol/LKHC2O4溶液中,下列关系正确的是 ( )
A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+ c(C2O42-)=0.1mol/L
C.c(C2O42-)﹤ c(H2C2O4)
D.c(K+)= c(H2C2O4)+c(HC2O4-)+c(C2O42-)
3.下列说法正确的是 ( )
A.pH=2和pH=1的硝酸中c(H+)之比为1:10
B.Na2CO3溶液c(Na+)与c(CO32-) 之比为2:1
C.0.2mol·L-1与0.1 mol·L-1醋酸中c(H+)之比为2:1
D.二氧化碳的饱和溶液中,c(H+)和c(CO32-)的比值为2:1
2.已知:灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
 Sn(s、灰)
Sn(s、白) △H>0; 下列说法正确的是 ( )
Sn(s、灰)
Sn(s、白) △H>0; 下列说法正确的是 ( )
A、白锡比灰锡稳定
B、在常温下锡以灰锡状态存在
C、灰锡转化为白锡的反应是放热反应
D、锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
1.下列说法正确的是
A.SO2的水溶液能导电,所以它属于电解质 ( )
B.纯净的水呈中性是因为纯水的离子积KW=1.0×10-14 ,PH=7的缘故
C.常温下,pH=1的水溶液中Na+、NO3-、HCO3-、Fe3+可以大量共存
D.为了避免青铜器生成铜绿,可将青铜器保存在干燥的环境中
18.(10分)在一固定体积的密闭容器中,在900℃时发生反应:
CH4(g)+H2O(g) CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
|
时间/min |
CH4 |
H2O |
CH3OH |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是 。
A.容器内压强不变 B.v正(H2)=v逆(CH4)
C.混合气体中CH3OH的浓度不变 D.c(CH3OH)=c(CH4)
(2)若在900℃时向反应容器中充入H2O,K值 (填“增大”“减小”或“不变”,下同);若升高反应体系的温度,K值 。
(3)上表中:c1= mol/L,H2O的转化率为 。
17.(12分)Ⅰ.下图是表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b
c过程中改变的条件可能是 ;
若增大压强时,反应速度变化情况画在c~d处。
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b
c过程中改变的条件可能是 ;
若增大压强时,反应速度变化情况画在c~d处。

Ⅱ.在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:
2A(g)+B(g) 3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度
3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度
(填“大于”“小于”或“等于”)。
(1)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度________Wmol·L-1。
(2)加入3 mol C和1 mol D时,C的平衡浓度_________Wmol·L-1。
(3)加入2 mol B、3 mol C、1 mol D时,C的平衡浓度_________Wmol·L-1。
16.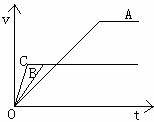 (6分)右图中A、B、C三条曲线分别表示足量的Na2CO3和
(6分)右图中A、B、C三条曲线分别表示足量的Na2CO3和
①100mL 2 mol/L盐酸②200mL 1 mol/L盐酸③400mL 0.8mol/L
盐酸反应时,反应时间t与产生CO2体积V的关系。由图可
以判断:A是Na2CO3和 盐酸的反应;B是Na2CO3和
盐酸的反应;C是Na2CO3和 盐酸的反应。(填
盐酸的序号)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com