
题目列表(包括答案和解析)
24.(18分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
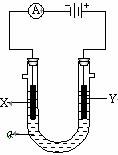
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为 。在X极附近观察到的现象是 。
② Y电极上的电极反应式为 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
① X电极的材料是 ,电极反应式是 。
② Y电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
23. (12分)已知反应AsO43-+2I-+2H+
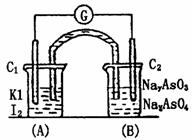
(12分)已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应.设计如图装置,进行下述操作:
AsO33-+I2+H2O是可逆反应.设计如图装置,进行下述操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安培表
指针偏转;
(Ⅱ)若改往(B)烧杯中滴加40%NaOH溶液,发现
微安培表指针向前述相反方向偏转.试回答:
(1)两次操作过程中指针为什么会发生偏转?
答:
。
(2)两次操作过程中指针偏转方向为什么会相反?试用平衡移动原理解释此现象.
答:
。
(3)(Ⅰ)操作过程中C1棒上发生的反应为 。
(4)(Ⅱ)操作过程中C2棒上发生的反应为 。
22.(20分)为省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4溶液;直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器(用品),以巧妙的构思,“接力”的方式,设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是 。甲同学的设计思路是 。
(2)乙同学接着甲的实验,向烧杯中滴加 溶液,进而观察到的现象是 , 。乙同学作出锌、铜金属活动性相对强弱所依据的原理是
, 。
(3)丙同学使用直流电源、石墨电极组装好电解装置,向乙同学实验后的溶液中补充了必要的试剂(作为电解液)。反应在调控下随即开始,实验中有关化学反应方程式为
。
获得的实验明显现象是 。
(4)请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌和铜的金属活动性的相对强弱(简要说明操作和现象)
。
21.(10分)将洁净的金属片Fe、Zn 、A、B 分别与Cu用导线连结浸在合适的电解质溶液里。实验并记录电压指针的移动方向和电压表的读数如下表所示:
|
金属 |
电子流动方向 |
电压/V |
|
Fe |
Fe
→ Cu |
+0.78 |
|
Zn |
Zn
→ Cu |
+1.10 |
|
A |
Cu
→ A |
-0.15 |
|
B |
B
→ Cu |
+0.3 |
根据以上实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越 (填“大”、“小”)。
Zn、A、B三种金属活动性由强到弱的顺序是 。
(2)Cu与A组成的原电池, 为负极,此电极反应式为
。
(3)A、B形成合金,露置在潮湿空气中, 先被腐蚀。
20.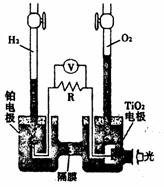 TiO2在光照射下可使水分解:2H2O
2H2↑+O2↑,该过程类似植物的光合作用。右图是光照射下TiO2分解水的装置示意图。下列叙述正确的是
TiO2在光照射下可使水分解:2H2O
2H2↑+O2↑,该过程类似植物的光合作用。右图是光照射下TiO2分解水的装置示意图。下列叙述正确的是
A.该装置可以将光能转化为电能,同时也能转化为化学能
B.铂电极上发生的反应为:2H++2e-=H2↑
C.该装置工作时,电流由TiO2电极经R流向铂电极
D.该装置工作时,TiO2电极附近溶液的pH变大
19.通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)︰n(硝酸亚汞)=2︰1,则下列表述 正确的是
A.在两个阴极上得到的银和汞的物质的量之比n(银)︰n(汞)=2︰1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的化学式为HgNO3
 D. 硝酸亚汞的化学式为Hg2(NO3)2
D. 硝酸亚汞的化学式为Hg2(NO3)2
18.某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl)︰n(H2SO4)
=3︰1。若以石墨电极电解该溶液,下列推断中不正确的是
A.阴极产物为H2 B.阳极先析出Cl2,后析出O2
C.电解液的pH不断增大,最终大于7
D.整个电解的过程实质是电解水
17.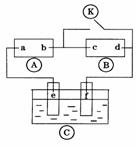 下图
下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现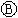 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通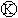 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是
A.a为直流电源的负极 B.c极发生的反应为2H++2e-=H2↑
C.f电极为锌板 D.e极发生氧化反应
16. 据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH
+ 3O2 + 4OH- 2CO32- + 6H2O,则下列说法错误的是
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH
+ 3O2 + 4OH- 2CO32- + 6H2O,则下列说法错误的是
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32- + 6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
15.当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是
A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成
B.电池的正极反应式为:O2 + 2H2O + 4e- = 4OH-
C.电解后c(Na2CO3)不变,且溶液中有晶体析出
D.电池中c(KOH)不变;电解池中溶液pH变大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com