
题目列表(包括答案和解析)
6.明矾(化学式为KAl(SO4)2·12H2O)是农村常用的一种净水剂,它在水中离解出K+、Al3+和SO42-。甲同学为了探究明矾中每种粒子是否有净水作用,进行了如下实验,请填写表中空白。
|
实验操作 |
实验现象 |
结论 |
|
在一杯浑浊的水中加少量KCl,静置 |
烧杯中的水仍浑浊 |
|
|
在一杯浑浊的水中加少量Al2(SO4)3,静置 |
烧杯中的水变澄清 |
|
乙同学看到甲的方案后,认为该方案不完善,他对甲同学的方案进行了补充完善。请你把乙同学补充方案中要达到的目的和所使用的试剂填入下表。
|
实验目的 |
使用的试剂 |
|
|
|
|
|
|
5.下图是1-18号元素原子最外层电子数与原子核电荷数的关系图。

试回答:
(1)一个水分子共有_______个原子核、____________个质子。
(2)一个Mg2+核外共有__________个电子;Cl-的最外层电子数和_________原子的最外层电子数相同。
(3)通过上图你能发现哪此规律?请写出其中一个:______________。
4.下图为四种粒子的结构示意图,请用对应的序号填空:
(1)属于同种元素的粒子是__________________________;
(2)具有相对稳定结构的粒子是__________________________;
(3)某元素R形成碱的化学式为R(OH)3,则R元素对应的原子结构示意图可能是____________。

3.根据粒子结构示意图给出的信息,下列说法正确的是( )
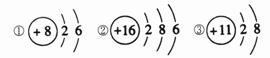
A.①②③表示的是三个原子 B.③表示的元素是非金属元素
C.①③表示的是阳离子 D.①②表示的元素化学性质相似
2.1个氢原子是由一个质子和一个电子构成,不含中子。当1个氢原子失去1个电子后,它不会变成( )
A.质子 B.原子核 C.阳离子 D.带负电荷的离子
1.现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜测其原因可能是( )
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁中含有OH- D.苹果汁中含有K+
2.对结构与性质之间的关系认识不清。结构决定了性质,反过来,性质又反映出结构。如例3。
[基础演练]
1.对原子、阳离子、阴离子的构成及其区别与联系,缺乏整体把握,造成错误。在原子中:核电荷数=质子数=电子数;在阳离子中:核电荷数=质子数>电子数;在阴离子中:核电荷数=质子数<电子数。如例2。
3.能从离子的角度描述物质的构成,能用粒子的观点解释一些现象和实验事实,如例3。
[典例精析]
例1:(威海市中考)在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。已知氢、碳、氧、钠、氯五种元素的核电荷数分别为:1、6、8、11、17。试按下列要求,写出微观粒子的化学符号,以及由这种粒子构成的或含有这种粒子的一种物质的名称(微观粒子和物质所涉及的元素限定在上述5种元素内)
|
需满足的条件 |
粒子的化学符号 |
对应的物质的名称 |
|
(1)质子数为11的同种元素的原子和离子 |
|
|
|
|
|
|
|
(2)质子数均为10的两种不同的分子 |
|
|
|
|
|
|
|
(3)质子数为1的阳离子和质子数为9的阴离子 |
|
|
|
|
|
解析 同元素的原子和离子指核电荷数相同,核外电子数不同的微粒。由于质子数为11,所以应是钠原子和钠离子;质子数均为10的不同的分子有NH3、H2O、HF、CH4等。质子数为1的阳离子是H+,质子数为9的阴离子有F-或者OH-。再找到含有这些离子的物质就可以了。
答案:
|
粒子的化学符号 |
对应物质名称 |
|
Na |
金属钠 |
|
Na+ |
氯化钠(氢氧化钠等) |
|
H2O |
水 |
|
CH4(HF、NH3) |
甲烷(氟化氢,氨气等) |
|
H+ |
盐酸(硫酸) |
|
OH-(F-) |
氢氧化钠(氟化氢) |
例2:(宜昌市中考)下列图示表示非金属元素的是 ;化学性质相似的是 ;具有稳定电子层结构的是 ;属于离子的是 ;表示同种元素的是 。


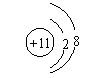
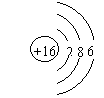
A. B. C. D.
解析 在原子结构示意图中,最外层电子数一般少于4个,为金属元素(H、He、B除外),多于或等于4个为非金属元素,等于8个为稀有气体元素(He为2个),上图中B、D最外层电子数大于4个,应为非金属元素;在原子结构示意图中,核内质子数等于核外电子数的为原子,不相等的则为离子,故A为离子;核内质子数相等的粒子为同种元素,最外层电子数相等的原子,化学性质也相似。
答案:表示非金属元素的是B、D、;化学性质相似的是B、D;具有稳定电子层结构的是B;属于离子的是A;表示同种元素的是A、C。
例3:(四川自贡课改区中考)下面这幅卡通画形象地展现了钠与氯气反应形成氯化钠的微观过程,在此过程中,钠原子变成了钠离子。

 钠与氯气反应形成氯化钠
钠与氯气反应形成氯化钠
(钠原子和氯原子的结构示意图分别为:
(1)钠元素处于元素周期表中的第_______周期;
(2)氯是非金属元素,它的原子在化学反应中一般比较容易_________电子;
(3)请你比较分析钠原子和钠离子的微粒结构的异同:
相同之处:___________________;不同之处:_____________________。
解析 根据题目所给信息及所学知识:原子的电子层数即为该元素在元素周期表中的周期数、元素的化学性质与原子最外层电子数的关系,(1)(2)两问较为简单。第(3)问主要结合离子形成的过程,从质子数、电子灵数、电子层数等方面入手,分析问题要全面、细致。
答案:(1)三(2)得到(3)核电荷数或质子数相同,第一、二层电子数相同,核外电子数、电子层数、最外层电子数不同。
[常见误区]
2.根据原子的结构来判断或推测元素相关的化学性质,如例2。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com