
题目列表(包括答案和解析)
20.(10分)I: (1分), (1分)
II:(1) 。(2分)
(2) (3分)
 (3)
(3分)
(3)
(3分)
19. (8分)
(8分)
⑴______________________ (2分)
⑵__________________ (2分)
⑶___________ (2分)
 ⑷__________
(2分)
⑷__________
(2分)
23.(14分)某药学杂志报道合成了一种具有明显抗癌活性的药物,其结构如下图所示。J是其同分异构体,J的合成路线如下(部分产物略去):
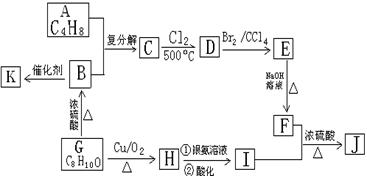
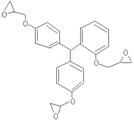
已知:① CH2=CHR1
+ CH2=CHR2  CH2=CH2 + R1CH=CHR2
CH2=CH2 + R1CH=CHR2
②R-CH2-CH=CH2 + Cl2 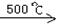 R-CHCl-CH=CH2 + HCl
R-CHCl-CH=CH2 + HCl
③核磁共振氢谱图显示A分子中不同环境氢原子个数比为3∶1;F是油脂水解的产物之一,能与水按任意比互溶;K是一种高分子化合物。
请回答下列问题:
(1)请写出A和G的结构简式:A ;G 。
(2)请写出下列反应的反应类型:G"B: ;C"D: 。
(3)写出下列反应方程式:B"K: ;F+I"J: 。
(4)同时满足下列条件的I的同分异构体有 种,请写出其中任意一种结构简式:
①分子中含有苯环结构;②能发生银镜反应;③苯环上的一氯代物有两种。

 单选题(3分×18=54分)
单选题(3分×18=54分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
非选择题(共56分)
22. (14分)已知:R-NH2或R1-NH-R2的性质与NH3相似,能与酸反应生成离子化合物。有机物A结构简式如下图所示:


有机物A在稀硫酸中受热会水解成B、C两种产物,B是一种离子化合物,C是一种共价化合物。
(1)A的分子式为 。在A的结构简式中虚线框内的结构名称为 。
(2)写出C跟碳酸氢钠反应的化学方程式 。
(3)C的同分异构体中,属于酚类也属于酯类的化合物有 种。
(4)某类有机物,属于C的同分异构体,分子中有苯环且苯环上连有三个取代基。写出这类有机物中含氧官能团的名称 。
(5)写出B跟过量氢氧化钠溶液加热的反应的离子方程式 。
21.(10分)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
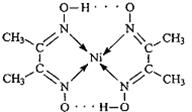 Ⅰ:配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体。
Ⅰ:配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体。
Ⅱ:配合物 分子内的作用力有 (填编号)。
 A.氢键 B.离子键 C.共价键 D.金属键
A.氢键 B.离子键 C.共价键 D.金属键
Ⅲ:氢气是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧(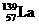 ) 和镍(
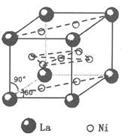
) 和镍(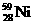 ) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,其他都在面上,镧原子在顶点上。储氢时氢原子存在于金属原子之间的空隙中。
) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,其他都在面上,镧原子在顶点上。储氢时氢原子存在于金属原子之间的空隙中。
(1)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为: 。
(2)下列关于该贮氢材料及氢气的说法中,正确的是 ( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
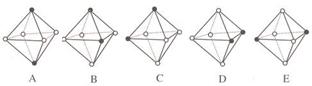
(3)Ni(CO)6为正八面体结构,镍原子位于正八面体的中心,配位体CO在正八面体的六个顶点上。若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是 。( 填字母编号,任填一组 )( 图中黑点为NH3,圆圈为CO,Ni略去)
20.(10分)Ⅰ:下列ΔH表示物质燃烧热的是 ,表示物质中和热的是 (填ΔH1、ΔH2、ΔH3等)。
A.2H2(g)+O2(g)=2H2O(l);ΔH1
 B.C(s)+1/2O2(g)=CO(g);ΔH2
B.C(s)+1/2O2(g)=CO(g);ΔH2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH3
D.C(s)+O2(g)=CO2(g);ΔH4
E.1/6C6H12O6(s)+O2(g)=CO2(g)+H2O(l);ΔH5
F.NaOH(s)+HCl(aq)=NaCl(aq)+H2O(l);ΔH6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l);ΔH7
H.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);ΔH8
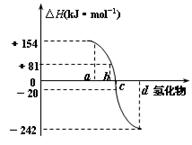
Ⅱ:已知:在298K、1.01×105Pa(标准热力学状态)下,
由稳定的单质发生反应生成1mol化合物的反应热叫该化合
物的生成热(△H)。右图为氧族元素氢化物a、b、c、d的
生成热数据示意图。试回答下列问题:
(1)写出氧族元素中含有18e-的两种氢化物的化学式 。
(2)请你归纳:非金属元素氢化物的稳定性与氢化物的反应热△H的关系 。
 (3)写出硒和氢气在热力学标准状态下,发生化合反应的热化学反应方程式
。
(3)写出硒和氢气在热力学标准状态下,发生化合反应的热化学反应方程式
。
19.(8分)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:
⑴先出现红褐色沉淀,原因是:______________________;
⑵随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式:__________________;
⑶最后溶液颜色加深,此过程的离子方程式是___________;
⑷如用稀盐酸代替HI稀溶液,能出现上述哪些相同的实验现象:__________(写序号)。
18.近年来,科学家发现由100个碳原子构成的一个具有完美对称性的C100原子团,其中
每个C原子仍可形成4个化学键。最内是由20个C原子构成的正十二面体,每个C原子与
相邻的3个C原子相连;外层的60个C原子形成12个分立的正五边形;处于中间层的C
将内外层的所有C连接在一起,当它与氢或氟在适当条件下充分反应时,其形成的分子式
应为
A.C100H20和C100F20 B.C100H60和C100F60
C.C100H12和C100F12 D.C100H40和C100F40
第Ⅱ卷 (非选择题共56分)
17.向胶体中加入电解质能使胶体聚沉。使一定量的液溶胶,在一定时间内开始聚沉所需电解质的浓度(mmol/L)称作聚沉值,电解质的聚沉值越小,则表示其聚沉能力越大,实验证明,聚沉能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,聚沉能力越大,则向Fe(OH)3溶液中,加入下列电解质时,其聚沉值最小的是:
A.NaCl B.FeCl3 C.K2SO4 D.Na3PO4
16.下列实验操作中,合理的是
A.实验室制取肥皂时,待植物油、乙醇和氢氧化钠溶液的混合物加热充分反应后,冷
却,用纱布滤出固态物质
B.实验室制乙烯时,在酒精和浓硫酸的混合液中,放入几片碎瓷片,加热混合物,使
液体温度迅速升到170℃
C.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置,待
液体分层后,滴加硝酸银溶液

 D.向淀粉在酸性条件下水解的产物中加银氨溶液,水浴加热,检验葡萄糖的生成
D.向淀粉在酸性条件下水解的产物中加银氨溶液,水浴加热,检验葡萄糖的生成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com