
题目列表(包括答案和解析)
23.(10分)在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应
H2(g)+I2(g)  2HI(g) △H<0。改变下列条件,反应速率将如何改变?(填“增大”“减
2HI(g) △H<0。改变下列条件,反应速率将如何改变?(填“增大”“减
小”或“不变”)
(1)升高温度 ; (2)加入催化剂 ;
(3)充入更多的H2 ; (4)扩大容器的体积 ;
(5)容器容积不变,通入氖气 。
22. (10分)一密闭容器中发生下列反应:
(10分)一密闭容器中发生下列反应:
N2(g)+3H2(g) 2NH3(g);ΔH<0
2NH3(g);ΔH<0
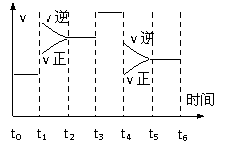
下图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题:
(1). t1、t3、t4时刻,体系中分别是什么条件发生了
变化?
__________________、______________________、 ____________________.
(2).下列时间段中,氨的百分含量最高的是_________.
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
21.(10分)在密闭容器中,通入amolN2和bmolH2,在一定条件下达到平衡,容器中还剩余cmolN2.
(1).生成NH3的物质的量为 .
(2).平衡时H2的转化率为 .
(3).若把容器体积减小一半,则正反应速率 ,逆反应速率 ,N2转化率 .(填“变大”、“变小”、或“不变”)
20.给蒸馏水中滴入少量盐酸后,下列说法中错误的是
A.[H+ ][OH- ]乘积不变 B.pH减小了
C.[OH- ]降低了 D.水电离出的[H+ ]增加了
请将选择题的答案填在下表中.( 每小题3分,共60分.)
19.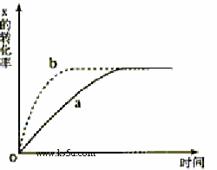 右图曲线a表示放热反应X(g)+Y(g)
右图曲线a表示放热反应X(g)+Y(g) 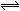 Z(g)+M(g)+N(g)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应的过程按b曲线进行,可采取的措施是
Z(g)+M(g)+N(g)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应的过程按b曲线进行,可采取的措施是
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
18. 在密闭容器中,对于反应:2SO2(g)+O2(g)  2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为
2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为
A.10 mol和10% B.20 mol和20%
C.20 mol和40% D.20 mol和80%
17.恒温恒压下,在容积可变的器皿中,反应2NO2(g) N2O4(g) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4(g) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.不变 B.增大 C.减小 D.无法判断
16.某温度下,在容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是 
A.均减半 B.均加倍 C.均增加2mol D.均减少2mol
15.可逆反应N2+3H2 2NH3的正逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
2NH3的正逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
A.3v正(N2)= v正(H2) B.v正(N2)= v正(NH3)
|
 C.2v正(H2)=3 v正(NH3) D.v正(N2)=3 v逆(H2)
C.2v正(H2)=3 v正(NH3) D.v正(N2)=3 v逆(H2)14.将pH=5的盐酸溶液稀释1000倍后,溶液的pH为
A.等于8 B.等于7 C.略小于7 D.略大于7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com