
题目列表(包括答案和解析)
2.在2H2+O2 2H2O反应中,_______份质量的氢气与_______份质量的氧气反应生成_______份质量的水,这三种物质之间的质量之比为_______。
2H2O反应中,_______份质量的氢气与_______份质量的氧气反应生成_______份质量的水,这三种物质之间的质量之比为_______。
答案:4 32 36 1∶8∶9
1.利用_________的化学方程式,才能进行计算,每个方程式各物质间都有固定的_________,质量比_________相等,但等号左右质量比之和_________相等,根据反应中的一种反应物或_________的质量,来计算另一种反应物或生成物的_________。在计算过程中要以_________定律为基础,利用正确的反应为依据。
答案:正确 质量比 不一定 一定 生成物 质量 质量守恒
3.分解反应
由________生成________________________________的化学反应,叫做分解反应。
答案:一种反应物 两种或两种以上其他物质
疑难突破
怎样选择制取气体的发生装置?
剖析:确定实验的发生装置主要依据反应物的状态和反应条件。①利用固体物质加热制取气体的发生装置用如图2-10中左图所示。②如果反应物是液体和固体而且不需加热制取气体时发生装置可采如图2-10中右图所示。
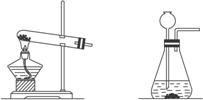
图2-10
问题探究
问题 如图所示,通常状况下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室常用加热氯化铵和消石灰的固体混合物制取氨气,请完成下列问题:
(1)实验室制取氨气的发生装置应选择什么发生装置?
(2)收集氨气,应采用的装置是什么?
探究:确定实验的发生装置主要依据反应物的状态和反应条件。若反应物是固体和固体,而且需要加热,就采用高锰酸钾制氧气的发生装置;若反应物是固体和液体而且不需加热,就采用过氧化氢溶液制氧气的发生装置。
而收集装置的选择主要依据生成物的性质,如密度是否比空气大,是否溶于水等。难溶于水或不易溶于水且不与水发生化学反应的气体适用于排水集气法;密度比空气大且不与空气中任何成分反应的气体适用于向上排空气法;密度比空气小且不与空气中任何成分反应的气体适用于向下排空气法。
典题精讲
例1 下列关于催化剂的叙述正确的是( )
A.能加快物质的化学反应速率的是催化剂,减慢化学反应速率的不是催化剂
B.加入二氧化锰可以使过氧化氢产生更多的氧气
C.催化剂在催化过程中所有的性质不变
D.同一个反应可以选用不同的催化剂
思路解析:对催化剂概念的理解是出错率最多的地方,很多同学往往把握不住催化剂定义的实质。根据催化剂的定义可知:“改变其他物质的化学反应速率”,“改变”既包括“加快”,也包括“减慢”之意,故A不对;在化学反应中,催化剂只能“改变其他物质的化学反应速率”,而对生成物的质量多少没有关系,故B错误;“二不变”是指催化剂在化学反应的过程中,质量和化学性质不变,而不是“性质”不变,因为物理性质可能改变,所以C不正确;同一个反应可以选用不同的催化剂,分解过氧化氢时还可以选用氧化铁、硫酸铜溶液作催化剂。
答案:D
例2 从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法是( )
A.通电使水分解:水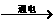 氢气+氧气
氢气+氧气
B.过氧化氢催化分解:过氧化氢 水+氧气
水+氧气
C.高锰酸钾加热分解:高锰酸钾加热锰酸钾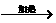 +二氧化锰+氧气
+二氧化锰+氧气
D.氯酸钾和催化剂加热分解:氯酸钾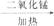 氯化钾+氧气
氯化钾+氧气
思路解析:实验室不用给水通电分解产生氧气的方法,成本高,速度慢。利用高锰酸钾和氯酸钾制取氧气时,需要加热,且还产生锰酸钾、氯化钾等物质,不如用过氧化氢催化分解,除产生氧气外就是水,不污染,且操作简便。
答案:B
知识导学
重点掌握氧气的实验室制法的反应原理和仪器装置,能够按照操作步骤制取氧气。
二氧化锰作催化剂是反应条件之一,故写在箭头的上方。
学习催化剂时注意:
①催化剂能改变其他物质的化学反应速率,这里的“改变”包括加快或减慢两种含义。
②催化剂的化学性质在化学反应前后没有改变,但是物理性质可能改变。
③催化剂是针对具体的反应而言的,如二氧化锰在过氧化氢分解制取氧气时,能够起催化作用,是催化剂;但二氧化锰不是所有化学反应的催化剂。
④在某个化学反应中,可以选择不同的物质作为催化剂。如利用过氧化氢分解制取氧气时,既可以选择二氧化锰作为催化剂,也可以选择氧化铁、硫酸铜溶液作催化剂。
⑤催化剂并不能增加产物的质量。
⑥催化剂可简单地理解为“一变二不变”。一变是指能改变其他物质的化学反应速率,这里的“改变”包括加快或减慢两种含义;二不变是指本身的质量和化学性质在化学反应前后都没有改变,但是物理性质可能改变。
收集装置的选择方法:
主要依据生成物的性质,如密度是否比空气大,是否溶于水等。
①排水集气法:适用于难溶于水或不易溶于水且不与水发生化学反应的气体。此法收集的气体较为纯净;当有大气泡从集气瓶口边缘冒出时,表明气体已收集满。
②向上排空气法:适用于相同状况下,密度比空气大且不与空气中任何成分反应的气体。操作时应注意将导管口伸到接近集气瓶底处,便于将集气瓶内的空气尽快地排尽。同时应在集气瓶的瓶口处盖上玻璃片,以便稳定气流。此法收集的气体较为干燥,但纯度较差,需要验满。
③向下排空气法:适用于相同状况下,密度比空气小且不与空气中任何成分反应的气体。操作时应注意将导管口伸到接近集气瓶底处,便于将集气瓶内的空气排尽。此法收集的气体较为干燥,但纯度较差,需要验满。
利用高锰酸钾制氧气时的注意问题:
①试管口要略向下倾斜,防止药品中的水分受热后变成水蒸气,再冷凝成水珠倒流回试管底部,使试管炸裂。
②导气管伸入试管内不要太长,只要露出橡皮塞少许即可,这样便于气体导出。
③药品不能聚集在试管底部,应平铺在试管底部,使之均匀受热。
④铁夹应夹在距离试管口约1/3处。
⑤要用酒精灯的外焰对准药品部位加热。加热时先进行预热,即先将酒精灯在试管下方来回移动,让试管均匀受热,然后对准药品部位加热。
⑥用排水法收集氧气时,导管口有气泡冒出时,不宜立即收集。因为刚开始排出的是空气,当气泡均匀连续地冒出时,才能收集。
⑦加热高锰酸钾制取氧气时,不要忘掉在试管;先预热,后集中在药品的部位加热;先将导管从,后熄灭酒精灯),也可缩记为:“查”“装”“定”“点”“收”“离”“熄”再利用谐音来理解记忆为:茶荘定点收利息。
口处放上一团松软的棉花,以免高锰酸钾小颗粒进入导气管,堵塞导气管。
⑧实验开始前,不要忘记检查装置的气密性。
⑨实验结束时,先把导气管从水槽中取出,再移走酒精灯,防止水倒流入试管底部炸裂试管。
⑩收集满氧气的集气瓶要盖好玻璃片,正放在桌子上(因为氧气的密度比空气大)。
氧气的工业制法的原理:
根据氧气和氮气的沸点不同分离出氧气。
在低温条件下加压,使空气转变为液态空气,然后蒸发。由于液态氮的沸点比液态氧的沸点低,因此氮气首先从液态空气中蒸发出来,剩下的主要是液态氧
分解反应可表示为AB A+B。
A+B。
注意生成物可以是两种或两种以上,反应物必须是一种。
疑难导析
要知道在初中阶段,制取气体的发生装置主要有哪些,确定实验的发生装置主要依据什么。
先要确定加热固体物质来制取气体,一般用什么反应容器,怎样连接,用什么仪器来加热,怎样固定反应容器。
然后确定反应物是液体和固体而且不需加热,一般用什么反应容器,怎样连接。
问题导思
关于确定实验的发生装置,要说明主要依据什么确定,分以下两种情况描述:
一是若反应物是固体和固体而且需要加热,要用什么发生装置。
二是反应物是固体和液体而且不需加热,要用什么发生装置。
关于收集装置的选择,要说明主要依据什么确定,分以下三种情况描述:
一是难溶于水或不易溶于水且不与水发生化学反应的气体适于用什么方法。
二是密度比空气大且不与空气中任何成分反应的气体适于用什么方法。
三是密度比空气小且不与空气中任何成分反应的气体适于用什么方法。
典题导考
黑色陷阱
催化剂有的可加快化学反应,有的可减慢化学反应,比较容易出错;在化学反应中,催化剂只能“改变其他物质的化学反应速率”,而对生成物的质量多少没有关系;同一个反应可以选用不同的催化剂。
典题变式
下列有关催化剂的叙述正确的是( )
A.在化学反应里能加快其他物质的化学反应速率,而本身质量和性质在反应前后都没改变的物质叫催化剂
B.二氧化锰是一切化学反应的催化剂
C.在过氧化氢的分解反应前后,二氧化锰的质量和化学性质都没有发生改变
D.要使过氧化氢分解放出氧气,必须加入二氧化锰,否则就不能发生反应
答案:C
绿色通道
比较几种制取氧气方法的利与弊,根据学过的旧知识,探究出新的知识,具体情况具体分析。
典题变式
为保证长时间潜航,在潜水艇里配备氧气再生装置,下列化学反应都能生成氧气,其中最适宜在潜水艇里供给氧气的反应是____________,与其他反应相比,它的优点是____________。
A.氯酸钾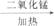 氯化钾+氧气
氯化钾+氧气
B.水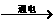 氢气+氧气
氢气+氧气
C.过氧化钠+二氧化碳 碳酸钠+氧气
碳酸钠+氧气
D.氧化汞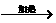 汞+氧气
汞+氧气
答案:C 原料易得,将人呼出的二氧化碳气体转化为氧气,该反应简便易行,不需加热和消耗电源,产物无毒
2.氧气的工业制法
工业上采用_____________的方法获得。

答案:分离液态空气
1.实验室制氧气
(1)在实验室里可用________溶液来制取氧气
①原理:(用文字表达式来表示)
过氧化氢 _________+__________
_________+__________
实验探究二氧化锰的作用:
|
实验编号 |
实验步骤 |
实验现象 |
实验结论 |
|
Ⅰ |
在试管中加入5 mL 5%的过氧化氢溶液,用带火星的木条伸入试管中 |
不复燃 |
在常温下过氧化氢溶液分解很慢 |
|
Ⅱ |
加热上述试管,用带火星的木条伸入试管中 |
有气泡冒出,木条复燃 |
温度升高,过氧化氢分解速率加快 |
|
Ⅲ |
在另一支试管中加入5 mL 5%的过氧化氢溶液,并加入少量二氧化锰,用带火星的木条伸入试管中 |
木条复燃 |
二氧化锰使过氧化氢分解速率加快 |
若在实验前准确称出二氧化锰的质量,实验后将二氧化锰回收、干燥、再称量,会发现它的质量__________改变。
结论:二氧化锰可使过氧化氢溶液在常温下迅速分解,作催化剂。
催化剂:在化学反应中能改变反应速率,但本身的________和________在反应前后都没有发生变化的物质。
②实验装置(发生装置、收集装置):
Ⅰ.发生装置的选择:由于过氧化氢是________,二氧化锰是________,且反应不需要________,故采用锥形瓶作为反应容器,配双孔胶塞,一孔插入分液漏斗,另一孔插入导管。
Ⅱ.收集装置的选择:由于氧气不易溶于水且不和水反应,故要制取较纯净的气体,需采用________法。又由于氧气的密度比空气的平均密度大,故要制取较干燥的气体时,需采用排________空气法。
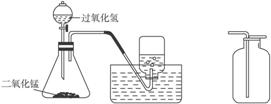
图2-8
③检验方法:
将带火星的木条伸入集气瓶中,如果,说明该瓶内的气体是氧气。
④验满方法:
Ⅰ.用排水法收集时,当气泡从_______冒出时,说明该瓶内的气体已满。
Ⅱ.用向上排空气法收集时,将带火星的木条放在_______处,如果木条复燃,说明该瓶内的气体已满。
⑤实验步骤:
Ⅰ.检查装置的_______;
Ⅱ.加药品(先加固体,后加液体);
Ⅲ.组装装置;
Ⅳ.收集氧气。
(2)在实验室中也可以用高锰酸钾来制取氧气
①原理:高锰酸钾 ________+________+氧气
________+________+氧气
②实验装置(发生装置、收集装置):
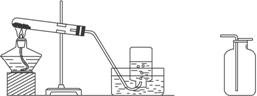
图2-9
③实验室用高锰酸钾制取氧气并用排水法收集的步骤。
实验室用高锰酸钾制取氧气并用排水法收集,其步骤可总结为“三先三后”(即先检查装置________,后装入_________,先预热,后集中在药品的部位加热;先将导管从_______,后熄灭酒精灯),也可缩记为:“查”“装”“定”“点”“收”“离”“熄”再利用谐音来理解记忆为:茶荘定点收利息。
答案:(1)①过氧化氢 水 氧气 没有 质量 化学性质
②液体 固体 加热 排水 向上
③木条复燃
④集气瓶外 集气瓶口
⑤气密性
(2)①锰酸钾 二氧化锰
③气密性 药品 水槽中取出
7.(1)硝酸钾的质量为:400Kg×7.1%=28.4Kg(2)硝酸钾中氮元素的质量分数为: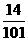 ×100%=13.9%,28.4Kg硝酸钾中氮元素的质量为:28.4Kg×13.9%=3.9Kg。
×100%=13.9%,28.4Kg硝酸钾中氮元素的质量为:28.4Kg×13.9%=3.9Kg。
6.硫酸钾(或K2SO4),氯化铵(或NH4Cl)
5.(1)氮、磷、钾;
(2)20kg;17.9 %
(3)方法一:分别取少量两种化肥,放在铁片上灼烧,若冒烟的是NH4Cl,无此现象的是K2SO4。方法二:分别取少量两种化肥于两支试管中,然后再加入蒸馏水,配成溶液,并分别滴加BaCl2溶液,有白色沉淀产生的是K2SO4,无此现象的是NH4Cl。方法三:分别取少量两种化肥于两支试管中,然后再加入熟石灰,加热,有刺激性气味气体放出的是NH4Cl,无此现象的是K2SO4。
1.B;2.B;3.B;4.A
7.(1)1.11﹪ (2) 符合
课题2答案:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com