
题目列表(包括答案和解析)
18、已知水在25℃和95℃时,
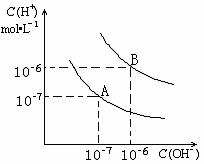 其电离平衡曲线如右图所示:
其电离平衡曲线如右图所示:
(1)则25 时水的电离平衡曲线应为
(填“A”或“B”),请说明理由
(2)25时,将=9的NaOH溶液与=4的溶液混合,
若所得混合溶液的 =7,则NaOH溶液与溶液的体积比为
(3)95时,若100体积1=的某强酸溶液与1体积2=b的某强碱溶液混合后
溶液呈中性,则混合前,该强酸的1与强碱的2之间应满足的关系是
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合
后,混合溶液的pH=5。请分析其原因:
17.据报道,我国拥有完全自主产权的氢氧燃料电池车将在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是( )
A.正极反应式为:O2+2H2O+4e- ===4OH-
B.工作一段时间后,电解液中的KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.1mol电子转移
Ⅱ 非选择题
16. 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2
+ 2Ni(OH)2
Cd(OH)2
+ 2Ni(OH)2
有关该电池的说法正确的是( )
A.充电时阳极反应:Ni(OH)2 -e- + OH- == NiOOH + H2O
班级 姓名
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
15. 取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是( )
取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是( )
 A.b电极是阴极 B.a电极与电源的正极相连
A.b电极是阴极 B.a电极与电源的正极相连
C.电解过程中水是氧化剂 D.b电极附近溶液的pH变小
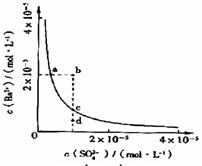
14.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成 D.a点对应的Ksp大于c点对应的Ksp
13.下列叙述正确的是( )
A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH的别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
 D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
12.反应2A(g) 2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是( )
2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是( )
A.升温 B.增大反应器的体积 C.增大c(A) D.降温
11.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2在相同温度下发生反应:2SO2+O2 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A等于p% B大于p% C小于p% D无法判断
10.能正确表示下列反应的离子方程式是[ ]
A.碳酸氢钙溶液和氢氧化钠溶液混合 HCO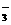 +OH
+OH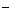 ==CO
==CO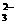 +H2O
+H2O
B.醋酸钠溶液和盐酸混合 CH3COONa+H+ == CH3COOH + Na+
C.少量金属钠放入冷水中 Na+ 2H2O== Na++2OH-+H2↑
D.硫酸铜溶液和氢氧化钡溶液混合 Cu2+ +
SO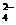 +Ba2+ + 2OH
+Ba2+ + 2OH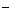 == Cu(OH)2↓+
BaSO4
== Cu(OH)2↓+
BaSO4
9.下列叙述正确的是[ ]
 A.95℃纯水的pH<7,说明加热可导致水呈酸性
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com