
题目列表(包括答案和解析)
2.下列金属的冶炼不适宜用热还原性来冶炼的是
A.铁 B.铜 C. 钠 D.铅
1.下列做法能改善空气质量的是
A. 以煤等燃料作为主要生活燃料
B.利用太阳能、风能和氢能等能源代替化石能源
C. 鼓励私人购买和使用汽车代替公交车
D.限制使用电动车
25.某强酸性工业废水中含有Fe2+、Fe3+、Cu2+,设计实验方案用沉淀法除去铁离子,得到较纯的Cu2+溶液。有关氢氧化物沉淀的pH如下表:
|
金属离子 |
pH |
|
|
开始沉淀 |
沉淀完全 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Cu2+ |
4.4 |
6.4 |
|
Fe3+ |
2.7 |
3.7 |
(1)从表中数据分析,为什么不能直接加NaOH将溶液pH调到9.6来除去Fe3+和Fe2+? 。
(2)实际应用中是先加一定量次氯酸钠,然后再调节pH。次氯酸钠的作用是什么? 。
(3)pH应调节到什么范围? 。 为什么? 。
(4)调节pH适宜的试剂是 (选填序号:A.氢氧化钡、B.碳酸镁、C.氧化铜、D.稀盐酸),理由是 。
答案.(1)如果直接将废水的pH从酸性调节到9.6,则铜离子也被沉淀掉,不符合题意要求(2)把Fe2+氧化成Fe3+,便于把铁杂质一次除去(3)3.7-4.4因为Fe3+在pH略大于3.7时就可完全转化为Fe(OH)3沉淀而被除去,在此pH下Cu2+尚没有开始生成沉淀 (4)C氧化铜能与溶液中的酸反应,使pH达到沉淀需要的范围,而且不引入新的杂质
24. 有效地利用现有能源和开发新能源已受到各国的普遍重视。
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH30C(CH3)3来生产“无铅汽油”。 CH30C(CH3)。分子中必存在的原子间连接形式有 (填写编号)
①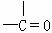 ②
②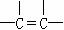 ③
③ ④
④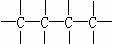
(2)天然气的燃烧产物无毒、热值高,而且管道输送方便,将成为我国西部开发的重点项目之一。天然气常和石油伴生,其主要的成分是 。能说明它是正四面体而非正方形平面结构的理由是 (填写编号)。
①其一氯取代物不存在同分异构体
②其二氯取代物不存在同分异构体
③它是非极性分子
④它的键长和键角都相等
答案:(1)③(2)甲烷②(3)③氢气的输送和贮存
23.收集多份淡水水样,如雨水、河水、池水、泉水、井水、自来水等,并从实验室取蒸馏水,进行下列实验,观察并记录现象。
|
实 验 内 容 |
蒸馏水 |
雨水 |
河水 |
井水 |
自来水 |
|
|
①过滤,看滤纸上是否有滤出物 |
|
|
|
|
|
|
|
②取滤出的清水,滴几滴在玻璃片上,小心烘干,比较玻璃片上的残留物的量 |
|
|
|
|
|
|
|
③取滤出液与明矾水混合,静置,看是否有沉淀 |
|
|
|
|
|
|
|
④取第①步滤出的水,与肥皂水混合,看是否有沉淀生成 |
|
|
|
|
|
|
答案.①过滤时,正常情况下除了河水可能有沉淀滤出,其余应该没有固体滤出; ②蒸馏水应没有残留,其他水样都会在玻璃片上留下残留物,除蒸馏水外,雨水最少,自来水次之,如果河水澄清,则应比井水少;③自然水包括井水中往往都有些悬浮杂质,故加明矾时会生成沉淀,蒸馏水和自来水不应有沉淀;④井水和河水含有钙、镁离子,加肥皂水生成沉淀注:因各自取样有特殊性,所以有些现象不一定都一样。
22、.农村还有些家庭直接用河水或池塘水作为生活饮用水,一般是把水担回家倒入水缸,加明矾使水澄清,加漂白粉进行消毒。明矾的化学式为 ,写出它溶于水后生成胶体的离子方程式: 。漂白粉的成分是 ,它在自然条件下能产生次氯酸,次氯酸的氧化性很强,能杀死病菌。写出漂白粉生成次氯酸的化学方程式: 。
答案.KAl(S04)2·12H20 Al3++3H2O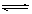 Al(OH)3(胶体)+3H+ CaCl2、Ca(C10)2
Al(OH)3(胶体)+3H+ CaCl2、Ca(C10)2
Ca(C10)2+C02+2H2O=CaC03↓+2HCl0
21.处理下列废水常用什么方法?将方法名称填在横线上。
(1)轧钢厂的含盐酸的废水: 。
(2)金矿的含氰化钠的废水: 。
(3)化工厂的含有能引起“痛痛病”的镉离子的废水: 。
答案.(1)中和法 (2)氧化还原法 (3)沉淀法
20、近年来,某些自来水厂在用液氯进行消毒处理时还加入少量液氨,其反应的化学方程式为 NH3+HclO=H2O+NH2Cl(一氯氨),NH2Cl较HClO稳定,试从化学平衡的观点分析液氨能延长液氯杀菌时间的原因:
答案:加入液氨后,它与HCl0结合成较稳定的一氯氨, HCl0浓度减小,使HClO跟别的物质反应的速率变慢,当HClO逐渐减少时,平衡向生成HCl0的方向移动,补充HCl0,使HClO在较长时间内保持一定的浓度
19、下列有关用03作自来水消毒剂的说法中,错误的是 ( )
A.利用了03的强氧化性杀菌
B.所用03是从高空臭氧层采取的,来源丰富
C. 03消毒可以避免液氯消毒有氯代烃生成的缺点,更符合卫生要求
D.O3消毒的自来水没有气味,消毒过程中也不生成污染物
答案.B
18.为了降低锅炉用水或化工用水的硬度,许多单位都应用离子交换柱。在此之前曾经普遍应用过“药剂法”,如石灰纯碱法等,使Ca2+、Mg2+转化成沉淀物从水中除去,达到软化硬水的目的。与之相比,离子交换法软化水的优点很多,下列各项中,不符合事实的是 ( )
A.操作简便,设备简单,占地面积小
B.离子交换剂(离子交换树脂或磺化煤)可再生,反复使用
C.能除去水中的所有离子
D.废水容易处理,不产生污染物
答案.C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com