
题目列表(包括答案和解析)
12.下列过程中△H<0的是 ( )
A. 氯酸钾分解制氧气 B. 实验室用氯化铵和氢氧化钙制氨气
C.煅烧石灰石制生石灰 D.盐酸与NaOH溶液反应
11.有一支 酸式滴定管,其中盛有溶液,液面恰好在
酸式滴定管,其中盛有溶液,液面恰好在 刻度处。把滴定管中的溶液全部排出,承接在量筒中,量筒内溶液的体积( )
刻度处。把滴定管中的溶液全部排出,承接在量筒中,量筒内溶液的体积( )
A. 大于40.00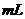 B. 为40.00
B. 为40.00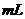 C. 小于
C. 小于 D. 为
D. 为
10.已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol·L-1、Ka(HF)= 6.8×10-4
mol·L-1、Ka(CH3COOH)=
1.8×10-5 mol·L-1、、Ka(HNO2)=
6.4×10-6mol·L-1  物质的量浓度都为0.1 mol·L-1的下列溶液中,pH最小的是
( )
物质的量浓度都为0.1 mol·L-1的下列溶液中,pH最小的是
( )
A.HCN B.HF C.CH3COOH D.HNO2
9.4份各2g的NaOH固体,分别加入100mL下列各液体中,待一定时间后(不计水分挥发)溶液的导电能力变化不大的是 ( )
A.自来水 B.0.5mol/LHCl
C.0.5mol/LCH3COOH溶液 D.0.5mol/L氨水
8. 在CH3COOH H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是
( )
在CH3COOH H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是
( )
A.加入NaOH B.加入盐酸 C.加水 D.升高温度
7.下列事实中,不能证明醋酸是弱酸的是 ( )
A.醋酸能使紫色石蕊试液变红 B. pH = 3的醋酸溶液稀释100倍后pH<5
C.醋酸钠溶液的pH>7 D.常温下,0.1 mol·L-1醋酸溶液pH=2.5
6.“熵”可看作是“混乱度”,它的符号是“S”。下列变化中,可以明显看出△S<0(“混乱度”减小)的是( )
A. 3Fe(s)+4H2O(g) = Fe3O4(s)+4H2(g) B.2NO2(g) = N2O4(l)
C.(NH4)2CO3(s) = 2NH3(g)+CO2(g)+2H2O(g) D.2IBr(l) = I2(s)+Br2(g)
5.对于反应2SO2(g)+O2(g) 2SO3
(g)能增大正反应速率的措施是
( )
2SO3
(g)能增大正反应速率的措施是
( )
A.通入大量O2 B.增大容器容积
C.移去部分SO3 D.降低体系温度
4.四个试管中都装有
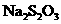 溶液,分别在不同温度下加入
溶液,分别在不同温度下加入 硫酸和一定量水,最先出现浑浊的是(
)
硫酸和一定量水,最先出现浑浊的是(
)
A.20℃,10 mL硫酸 B.20℃,5 mL硫酸,5 mL水
C.30℃,5 mL硫酸,2 mL水 D.30℃,4 mL硫酸,3 mL水
3.下列物质的稀水溶液中,除水分子外,不存在其它分子的是 ( )
A.NH4Cl B.NaHSO3 C.HNO3 D.HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com