
题目列表(包括答案和解析)
22.能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是 ( )
A.向水中投入一小块金属钠 B.将水加热煮沸
C.向水中加入硝酸铵晶体 D.向水中加食盐晶体
21.下列关于电解质溶液的叙述中正确的是 ( )
A.Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同
B.在CH3COONa溶液中c (CH3COO-) > c(Na+) > c(OH-) > c(H+)
C.在0.1mol·L-1的醋酸溶液中加入适量的蒸馏水,溶液的c(H+)/c(CH3COOH)增大
D.常温下,某溶液中由水电离出的c(H+)为10-5 mol/L,则此溶液可能是盐酸
20.下列各组离子一定能在指定环境中大量共存的是 ( )
A.在c(H+)=10-10
mol/L的溶液中 Al3+
、NH 、Cl- 、NO
、Cl- 、NO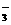
B.pH值为1的溶液 Fe3+、Na+ 、SO42-、HCO3-
C.水电离出来的c(H+)=10-12mol/L的溶液 K+、NH4+、Cl-、ClO-
D.pH值为13的溶液
K+ 、SO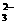 、Na+、AlO2-
、Na+、AlO2-
19.某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH<0
2Z(g);ΔH<0
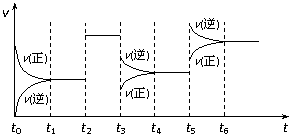
上图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
A.t2时增大了压强 B.t3时降低了温度
C.t5时加入了催化剂 D.t6时反应物的转化率比t4时低
18.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
 HIn(溶液) H+(溶液)+
In-(溶液)
HIn(溶液) H+(溶液)+
In-(溶液)
红色 黄色
浓度为0.02 mol·L-1的下列各溶液: ①盐酸 ②石灰水 ③NaCl溶液 ④NaHSO4溶液
⑤NaHCO3溶液 ⑥氨水,其中能使指示剂显红色的是 ( )
A.①④⑤ B.②⑤⑥ C.①④ D.②③⑥
17.在25℃进,浓度均为1 mol·L-1的(NH4)2SO4、(NH4)2C2O4、(NH4)2Fe(SO4)2三种溶液中,测得其中c(NH4+)分别为a mol·L-1、b mol·L-1、c mol·L-1,则下列判断正确的是 ( )
A.a > b > c B.c > a > b C.b > a > c D.a > c > b
16.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)  2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是 ( )
2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是 ( )
A.a>b B.a=b C.a<b D.无法确定
15.在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g) 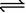
 N2(g)+CO2(g);△H=-373.2kJ·mol-1
,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g);△H=-373.2kJ·mol-1
,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
14. 在一定温度下,向一容积不变的密闭容器中加入1 mol X气体和2mol Y气体,发生如下反应: X(g)
+ 2Y(g) 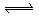 2Z(g) , 此反应达到平衡的标志是 (
)
2Z(g) , 此反应达到平衡的标志是 (
)
A.容器内压强不随时间变化
B.容器内气体密度不随时间变化
C. 容器内X、Y、Z的浓度之比为l : 2 : 2
D.单位时间消耗0.1 mol X同时生成0.2 mol Z
13.已知两个热化学方程式: C(s)+O2(g)==CO2(g) △H = -393.5kJ/mol
2H2(g)+O2(g)==2H2O(g) △H = -483.6kJ/mol
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是 ( )
A.1:1 B.1:2 C.2:3 D.3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com