
题目列表(包括答案和解析)
14. 在一定温度下,向AgI的饱和溶液中:(填“增大”、“减小”或“不变”)
(1)若加入AgNO3固体,c(I-) 。
(2)若加入更多的AgI固体,则c(Ag+) 。
(3)若加入固体AgBr,c(I-) 。
32.在2L的密闭容器中充入2mol的CO和2mol H20,800 0C时反应达到平衡:
CO(g)_+H20(g) C02(g)+H2(g),此时平衡常数K=1,求:
C02(g)+H2(g),此时平衡常数K=1,求:
①CO的转化率;②若温度不变,再通入16mol H20(g),则CO的总转化率比以前大了还是减少了?通过计算回答。

31.(10分)工业上制备H2的一种重要方法是:CO(g)+H2O(g)  C02(g)十H2(g)△H=Q kJ·mol-1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850℃时发生上述反应:并测得容器内各物质的浓度(mol·L-1)随时间的变化关系如下表:
C02(g)十H2(g)△H=Q kJ·mol-1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850℃时发生上述反应:并测得容器内各物质的浓度(mol·L-1)随时间的变化关系如下表:
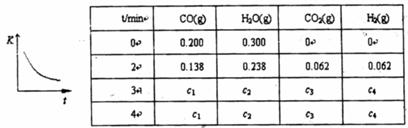
已知:8500C时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是 。
A.单位时间内减少CO(g)的浓度等于生成C02(g)的浓度
 B.反应容器内的压强不发生变化
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q 0(填“>”、“=”或“<”)。 ,
(3)若在850℃时向反应容器中充入H20(g),K值 (填“增大”、“减小’’或“不变”)。
(4)上表中c2为 m01.L-1,CO(g)的转化率为 。
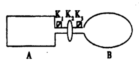
30. (12分)A是由导热材料制成的密闭容器,B是_耐化学腐蚀且易于传热的气球。关闭IK2,将等量且少量的NO2通过K1、K2分别充人A、B中,反应起始时,A、B的体积相同。(已知:
(12分)A是由导热材料制成的密闭容器,B是_耐化学腐蚀且易于传热的气球。关闭IK2,将等量且少量的NO2通过K1、K2分别充人A、B中,反应起始时,A、B的体积相同。(已知: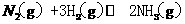 ;△H<0)
;△H<0)
(1)一段时间后,反应达到平衡,此时A、B中生成的N204的速率是VA VB。(填“>”、“<”、“=”);若打开活塞K2,气球B将 (填:变大、变小、不变)。
 (2)若在A、B中再充人与初始量相等的N02,则达到平衡时,N02的转化率aA将
(填增大或减小、不变);若通入等量的Ne气,则达到平衡时,
(2)若在A、B中再充人与初始量相等的N02,则达到平衡时,N02的转化率aA将
(填增大或减小、不变);若通入等量的Ne气,则达到平衡时,
A中NO2的转化率将 ,B中NO2的转化率将
(填:变大、变小、不变)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,
B与外界可以进行热传递,则达到平衡时, 中的颜色较深。
29.(10分)在一个盛有催化剂容积可变的密闭容器中,保持一定温度和压强,进行以下反应:
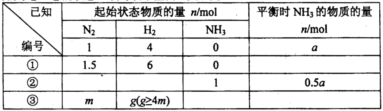
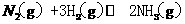 。已知加入lmol N2和4mol H2时,达到平衡后生成a mol NH3(见下表已知项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①-③的状态,填写表中空白(共5处)。
。已知加入lmol N2和4mol H2时,达到平衡后生成a mol NH3(见下表已知项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①-③的状态,填写表中空白(共5处)。
28.(8分)(填序号)下列物质能导电的是 ,属于强电解质的是
属于弱电解质的是 ,属于非电解质的是 。
a.铝片 b.石墨 c.KN03晶体 d.盐酸 e.蔗糖 f.C02
g.Na2O h.冰醋酸 i.碳酸氢铵 j.NH3 k.BaS04
27.(8分)甲、乙两容器,甲的容积固定,乙的容积可变。在一定温度下,向甲中通入3mol N2和4mol H2,反应达到平衡时,生成NH3的物质的量为amol。
 (1)相同温度下,向乙中通入2molNH3,且保持容积与甲相同,当反应达到平衡时,各物质的浓度与甲平衡中相同。起始时乙中还通入了 mol N2和 mol H2。
(1)相同温度下,向乙中通入2molNH3,且保持容积与甲相同,当反应达到平衡时,各物质的浓度与甲平衡中相同。起始时乙中还通入了 mol N2和 mol H2。
(2)相同温度下,若向乙中通入6mol N2和8mol H2,且保持压强与甲相等,当反应达到平衡时,生成氨的物质的量为b mol,则a:b 1:2:若乙与甲的容积始终相等,达到平衡时,生成氮的物质的量为c mol,则a:c 1:2(填“>“<"或“=’’),
26.(6分)今有a.盐酸 b·硫酸c·醋酸三种酸(用序号填):
①在同体积,同pH的三种酸中,分别加入足量的碳酸钠粉末,在相同条件下产生C02的体积由大到小的顺序是 。
②在同体积、同浓度的三种酸中,分别加入足量的碳酸钠粉末,在相同条件下产生C02的体积由大到小的顺序是 。
③物质的量浓度均为0.1 mo1.L-l的三种酸溶液的pH由大到小的顺序是 。
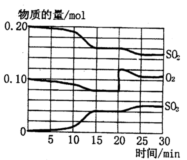
25.(12分)一定条件下,将S02和02充入一密闭容器
中,发生如下反应:2S02(g)+O2(g)  2SO3(g),△H<0。
2SO3(g),△H<0。
反应过程中S02、02、S03物质的量变化如图所示:回答、
下列问题:
(1)若降低温度,该反应的化学平衡常数 ,
二氧化硫转化率 ,化学反应速率
。(填“增大’’‘‘减小’’或“不变’)
(2)该反应处于平衡状态的时间段为 .
 (3)反应进行至20 min时,曲线发生变化的原因是
(用文字表达)。10 min到15 min的曲线变化的原因可能是
(填写编号)。
(3)反应进行至20 min时,曲线发生变化的原因是
(用文字表达)。10 min到15 min的曲线变化的原因可能是
(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加S02的物质的量
24、将固体NH4I置于密闭容器中,在某温度下发生下列反应:
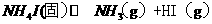 ,
,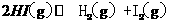 ,当达到平衡时,C(H2)=0.5mol/L,C(HI)=4mol/L,则NH3的浓度为
,当达到平衡时,C(H2)=0.5mol/L,C(HI)=4mol/L,则NH3的浓度为
A.3.5mol/L B.4mol/L C、4 5mol/L D.5mol/L. …
 第Ⅱ部分:非选择题(72分)
第Ⅱ部分:非选择题(72分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com