
题目列表(包括答案和解析)
5.钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A. 2H++2e-=H2 B. Fe2++2e-=Fe
B. 2H2O+O2+4e-=4OH- D. Fe3++e-=Fe2+
4.下列各变化中属于原电池反应的是
A.在空气中金属铝表面迅速氧化形成保护层
B.镀锌铁表面有划损时,也能阻止铁被氧化
C.红热的铁丝与冷水接触,表面形成蓝黑色保护层
D.浓硝酸比稀硝酸更能氧化金属铜
3.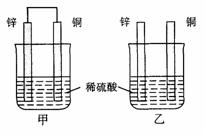 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
2. 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O
由此可知,该电池放电时的负极材料是
A.Cd(OH)2 B.Ni(OH)2 C.Cd D.NiO(OH)
1.废电池的污染引起人们的广泛重视,废电池中对环境形成污染的主要物质是
A.锌 B.汞 C.石墨 D.二氧化锰
5.[江苏省江宁、江浦、六合三校2009届高三上学期1月联考化 学](14分)不同的金属在化学反应中表现出来的活泼程度不同,早在1812年瑞典化学家贝采里乌斯根据大量实验现象首先提出了金属活动顺序的概念,后来俄国化学家贝开托夫在大量实验和系统研究之后,于1865年发表了金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 。
(1)金属活动性顺序是学习“金属及其化合物”的重要工具,许多“金属及其化合物”的知识规律可以通过金属活动性顺序来掌握。例如,工业上冶炼金属,根据金属活动性顺序可以采用不同的冶炼方法。其中可以用“热分解法”冶炼的金属是 、 。
 工业上又常用下列反应进行金属钾的冶炼:
,似乎“违背”了金属活动性顺序,试解释钠能将更活泼的钾置换出来的原因
。
工业上又常用下列反应进行金属钾的冶炼:
,似乎“违背”了金属活动性顺序,试解释钠能将更活泼的钾置换出来的原因
。
(2)在实践中发现还有许多化学事实 “违背”金属活动性顺序,但这些“反常”现象都可以通过化学原理得到合理解释。某学生在做探究实验时,把锌粒投入1mol·L-1氯化铁溶液中,观察到如下实验现象:锌粒表面有一定量气泡产生,溶液颜色逐渐变浅,一段时间后溶液逐渐浑浊,试用相关反应方程式进行解释 、 。
(3)研究金属活动性顺序还可以指导对金属阳离子氧化性强弱的认识,工业上用氯化铁溶液腐蚀铜制电路板。
①请根据金属活动性顺序结合该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性强弱 。
②请运用原电池原理设计实验验证Cu2+、Fe3+氧化性强弱的结论。
方案及现象: 。
4.
 [盐城市2008/2009学年度高三年级摸底考试]竖炉冶铁工艺流程如图,使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧CH4(g)+2O2(g)=CO2(g)+2H2O(g),催化反应室发生的反应为:CH4(g)+H2O(g)
[盐城市2008/2009学年度高三年级摸底考试]竖炉冶铁工艺流程如图,使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧CH4(g)+2O2(g)=CO2(g)+2H2O(g),催化反应室发生的反应为:CH4(g)+H2O(g)
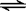 CO(g)+3H2(g)
∆H1=+216kJ/mol;CH4(g)+ CO2(g)
CO(g)+3H2(g)
∆H1=+216kJ/mol;CH4(g)+ CO2(g)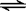 2CO(g)
+ 2H2(g) ∆H2=+260kJ/mol(不考虑其他平衡的存在),下列说法正确的是[A]
2CO(g)
+ 2H2(g) ∆H2=+260kJ/mol(不考虑其他平衡的存在),下列说法正确的是[A]
A.增大催化反应室的压强,甲烷的转化率减小
B.催化室需维持在550-750℃,目的仅是提高CH4转化的速率
C.设置燃烧室的主要目的是产生CO2和水蒸气作原料气与甲烷反应
D.若催化反应室中,达到平衡时,容器中n(CH4)=amol/L,n(CO)=bmol/L
n(H2)=cmol/L,则通入催化反应室的CH4的物质的量为a+(b+c)/4
3、[启东市汇龙中学2008-2009学年度高三年级下第三次模拟]用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是[BD]

A.电池工作时,正极反应式为O2 + 2H2O + 4e- == 4 OH-
B.电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量消耗,当电池中消耗0.02g H2时,b极周围会产生0.02g H2
2.[江苏省无锡市2009届高三上学期期末调研考试]肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%-30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是[AD]
A.负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2↑
B.正极的电极反应式是:O2+4H++4e-=2H2O
C.溶液中阴离子向正极移动
D.溶液中阴离子物质的量基本不变
1. [江苏省南通市08-09年度第二学期九校联考高三化学试卷 09.3]设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一。最近有人设计了一种固体燃料电池,固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是[BD]
[江苏省南通市08-09年度第二学期九校联考高三化学试卷 09.3]设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一。最近有人设计了一种固体燃料电池,固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是[BD]
A.b极为电池的正极
B.b极对应的电极反应式为:
C5H12+16O2--32e-=5CO2+6H2O
C.该电池的总反应方程式为:C5H12+8O2+10OH-=5CO32-+11H2O
D.汽油燃料电池最大的技术障碍是氧化反应不完全,产生炭粒堵塞电极的气体通道,从而使输电效能减弱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com