
题目列表(包括答案和解析)
19.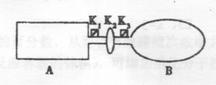 A是由导热材料制成的密闭容器,B是一耐化学腐
A是由导热材料制成的密闭容器,B是一耐化学腐
 蚀且易于传热的气球.关闭K2,将等量且少量的
蚀且易于传热的气球.关闭K2,将等量且少量的
NO2通过K1、K3分别充入A、B中,反应开始时,
A、 B的体积相同。已知:
2NO2(g) N2O4(g) △H<0。
N2O4(g) △H<0。
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是V(A) V(B)(填“<”、“>”或“=”);若打开活塞K2,气球B将 (填“变大”、“变小”或“不 变”,下同)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将 ;
若通入等量的Ne气,则达到平衡时,A中NO2的转化率将 ,B中NO2的转化率将 。
(3)室温时,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深。
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为 。
18.在2L的密闭容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)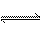 2C
2C
(g)+D(s),达到平衡时,C的浓度为0.4mol·L-1。
(1)温度不变,若缩小容器体积,则平衡 移动(填“正向”、“逆向”、“不”)。
(2)维持容器的温度和体积不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是0.4mol·L-1的是 。
A、4molA+2molB B、2molC+1molD
C、2molA+1molB+2molC+1molD D、1molA+0.5molB+1molC+0.2molD
 (3)若维持容器的温度和体积不变,按不同配比加入起始物质,达到平衡时, C的浓度仍是0.4mol·L-1。
(3)若维持容器的温度和体积不变,按不同配比加入起始物质,达到平衡时, C的浓度仍是0.4mol·L-1。
①反应从逆反应开始,则D的起始物质的量应满足的条件是 。
②若加入0.2molA和0.1molB,则C和D起始物质的量分别应满足 、 。
17.在一定温度下,有1mol N2气体和3mol H2气体发生下列反应:
N2(g)+3H2(g) 2NH3(g) △H<0。
2NH3(g) △H<0。
(1)若在相同温度下,分别在1L定压密闭容器A中和1L定容密闭容器B中反应:
哪个容器中的反应先达到平衡? 答: 。
哪个容器中的N2的转化率高? 答: 。
(2)若在上述定压密闭容器A中,反应已达到平衡时,再加入0.5摩氩气,则N2的
转化率会起什么变化?答: 。
正反应速度与原平衡相比,有无变化,简答理由。
。
(3)若在1L定容容器中,上述反应达到平衡时,平衡混和物中N2、H2、NH3的物质
的量分别为A、B、C摩。仍维持原温度,用x、y、z分别表示开始时N2、H2、NH3
的加入的物质的量(mol),使达到平衡后N2、H2、NH3的物质的量也为A、B、C摩。则应满足的条件是:
①若x=0,y=0,则z= 。
②若x=0.75,则y应为 mol、z应为 mol。
③x、y、z应满足的一般条件是 。
16. 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是 ( )
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是 ( )
A.CH3OH(l) + 3/2O2(g) == CO2(g) + 2H2O(l);△H=+725.8kJ/mol
B.2CH3OH(l) + 3O2(g) == 2CO2(g) + 4H2O(l);△H=-1452kJ/mol
C.2CH3OH(l) + 3O2(g) == 2CO2(g) + 4H2O(l);△H=-725.8kJ/mol
D.2CH3OH(l) + 3O2(g) ==2 CO2(g) + 4H2O(l);△H=+1452kJ/mol
15.下列说法正确的是 ( )
A.增大压强,活化分子百分数增大,化学反应速率一定增大
 B.升高温度,活化分子百分数增大,化学反应速率一定增大
B.升高温度,活化分子百分数增大,化学反应速率一定增大
C.加入反应物,使活化分子百分数增大,化学反应速率增大
D.使用催化剂,降低了反应的活化能,增大了活化分子百分数,反应速率一定增大
14.下列有关叙述中正确的是 ( )
A.难溶于水的电解质一定是弱电解质
B.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强
C.易溶于水的电解质一定是强电解质
D.强电解质在水溶液中的电离过程是不可逆的
13.用物质的量都是0.1molCH3COOH和CH3COONa配制成1L混合液,已知其中C(CH3COO-)大于C(Na+),对该混合物溶液的下列判断正确的是 ( )
A.C(H+)>C(OH-)
B.C(CH3COO-)+C(CH3COOH)=0.2mol/L
C.C(CH3COOH)>C(CH3COO-)
D.C(CH3COO-)+C(OH-)=0.1mol/L
12. 在密闭容器,一定条件下进行反应,mA(g)+nB(g)
在密闭容器,一定条件下进行反应,mA(g)+nB(g)
 pC(g)+qD(g) 若增大压强或升高温度,重新达到
pC(g)+qD(g) 若增大压强或升高温度,重新达到
平衡,变化过程均如图所示,则对该反应叙述正确的是
A.正反应是吸热反应
B.逆反应是吸热反应
C.m+n>p+q
D.m+n<p+q
11.pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)
 的关系如图示,下列说法不正确的是 ( )
的关系如图示,下列说法不正确的是 ( )
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
10.镍镉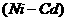 可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:



 由此可知,该电池放电时的负极材料是 ( )
由此可知,该电池放电时的负极材料是 ( )
A.  B.
B. 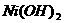 C.
C.  D.
D. 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com