
题目列表(包括答案和解析)
4.当两极都用银片作电极电解AgNO3溶液时,在阳极上的产物是( )
A.只有银 B.银和氧气
 C.只有氢气 D.上述都不对
C.只有氢气 D.上述都不对
3.电解水时为了增强其导电性不应加入的电解质是( )
A.NaOH B.CuSO4 C.H2SO4 D.KNO3
2.下列关于铜电极的叙述正确的是( )
A.铜锌原电池中铜是负极
B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时可用金属铜作阳极
D.电解稀硫酸制H2、O2时铜作阳极
1.用石墨作电极,电解1mol·L-1下列物质的溶液,溶液的pH保持不变的是( )
A.HCl B.NaOH C.Na2SO4 D.NaCl
14.根据可逆反应: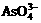 +2I-+2H+
+2I-+2H+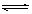
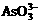 +I2+H2O,设计如下图所示实验装置。B烧杯中装有Na3AsO4和Na3AsO3溶液,A烧杯中装有I2和KI溶液。两烧杯中用一倒置的装有饱和KI溶液的U型管相连,该装置称为盐桥,其作用是避免两烧杯中的溶液相混合,又能使两烧杯中的溶液因相连通而导电。C1、C2棒为惰性电极。进行如下操作:
+I2+H2O,设计如下图所示实验装置。B烧杯中装有Na3AsO4和Na3AsO3溶液,A烧杯中装有I2和KI溶液。两烧杯中用一倒置的装有饱和KI溶液的U型管相连,该装置称为盐桥,其作用是避免两烧杯中的溶液相混合,又能使两烧杯中的溶液因相连通而导电。C1、C2棒为惰性电极。进行如下操作:
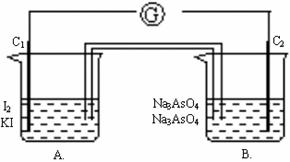
(1) 向A溶液中逐滴加入浓盐酸,发现电流计指针发生偏转。
(2) 若改向B溶液中滴加40%的 NaOH溶液,发现电流计指针向相反方向偏转。
试回答以下问题:
(1) ① 两次操作中,电流计指针偏转方向相反,为什么?试用化学平衡原理解释之 。② (1)操作过程中,C1棒上发生的反应是 。
(2) 操作过程中C2上发生的反应是 。

______年______月______日 星期_______
13.用Pt电极电解pH=6的R(NO3)2溶液600mL,当其中一极生成标准状况下672mL气体时,另一极增重3.81g,忽略溶液体积变化,则R的相对原子质量为多少?
12.有一硝酸盐晶体,化学式为M(NO3)x·nH2O,经测定知相对分子质量为242。将2.42g该晶体溶于水配成200mL溶液,将此溶液置于装有惰性电极的电解池中进行电解。若有0.02mol电子转移给金属离子时,溶液中金属离子全部析出,经称量,阴极增重0.64g。试计算:
(1)金属M的相对原子质量及x和n的值各是多少?
(2)若电解时溶液体积变化可忽略不计,则电解后溶液的pH是多少?

11.工业上为了处理含有Cr2O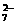 的酸性工业废水,采用如下处理方法:往工业废水中加入适量的食盐(NaCl),然后以铁为电极通直流电进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3生成,废水可达排放标准。简要回答下列问题:
的酸性工业废水,采用如下处理方法:往工业废水中加入适量的食盐(NaCl),然后以铁为电极通直流电进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3生成,废水可达排放标准。简要回答下列问题:
(1)阳极和阴极发生的电极反应是什么?
(2)写出Cr2O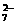 变为Cr3+的离子方程式,并说明生成Cr(OH)3、Fe(OH)3等难溶化合物的原因。
变为Cr3+的离子方程式,并说明生成Cr(OH)3、Fe(OH)3等难溶化合物的原因。
(3)能否用石墨电极代替铁电极达到电解铬的目的?为什么?
10.实验室用蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb+SO ===PbSO4+2e- 正极:PbO2+4H++SO
===PbSO4+2e- 正极:PbO2+4H++SO +2e-===PbSO4+2H2O,今若制得Cl20.05mol,这时电池内消耗的H2SO4的物质的量至少是
+2e-===PbSO4+2H2O,今若制得Cl20.05mol,这时电池内消耗的H2SO4的物质的量至少是
A.0.025mol B.0.050mol C.0.10mol D.0.20mol
9.柯尔贝反应是:2RCOOK+2H2O R-R+H2↑+2CO2↑+2KOH(R代表烃基),则下列说法正确的是
R-R+H2↑+2CO2↑+2KOH(R代表烃基),则下列说法正确的是
A.含碳元素的产物均在阳极区生成
B.含碳元素的产物均在阴极区生成
C.含氢元素的产物均在阳极区生成
D.含氢元素的产物均在阴极区生成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com