
题目列表(包括答案和解析)
16.在1L 0.3 mol·L-1的NaOH溶液中通入标准状况下CO2 4.48L,恰好完全反应,则下列关系式中,正确的是 ( )
A.c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)
B.c(Na+)> c(HCO3-) >c(CO32-) >c(OH-)
C.c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
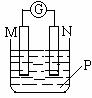 D.c(Na+
)+c(H+)=c(OH-) + c(CO32-) + c(HCO3-)
D.c(Na+
)+c(H+)=c(OH-) + c(CO32-) + c(HCO3-)
15.在强酸性环境中,下列各组离子能大量共存的是 ( )
A. NH4+、Cl-、NO3-、 Fe2+
B.Fe3+、 ClO-、Na+、SO42-
C. SO42-、Cl-、Na+、Fe3+
D. SO32-、S2-、Na+、K+
14.室温下,将pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液pH=11,则混合时强碱与强酸溶液的体积比是( )
A.11∶1 B.9∶1 C.1∶11 D.1∶9
13.可逆反应:3A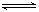 3B+C,△H>0 ,已知反应物A为气态物质,随着温度升高,反应体系中气体的平均相对分子质量有变小趋势,则下列判断中,正确的是 ( )
3B+C,△H>0 ,已知反应物A为气态物质,随着温度升高,反应体系中气体的平均相对分子质量有变小趋势,则下列判断中,正确的是 ( )
① B和C可能都是固体 ②B和C一定都是气体
③ 若C为固体,则B一定是气体 ④ B和C可能都是气体
A.①② B. ②③ C.①④ D.③④
12. 0.3mol的气态高能燃料乙硼烷B2H6在O2中燃烧,生成固态B2O3和液态H2O, 放出649.5kJ的热量。又知H2O(l) = H2O(g) △H=+44kJ /mol
下列热化学方程式中,正确的是 ( )
A. B2H6(g)+3O2(g)==B2O3(s)+3H2O(l) △H =+2165kJ /mol
B. B2H6(g)+3O2(g)==B2O3(s)+3H2O(g) △H =-2033kJ /mol
C. B2H6+3O2 ==B2O3+3H2O △H =-2165kJ /mol
D. B2H6(g)+O2(g)==B2O3(s)+H2O(g) △H =-2165kJ /mol
11.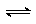 有可逆反应mA(s)+nB(g) pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的
有可逆反应mA(s)+nB(g) pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的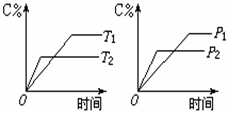 是 B
是 B
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应方向移动
C.平衡后增大A的量,有利于提高A的转化率
D.化学方程式中一定是n>p+q
10.只用一种试剂就可以鉴别FeCl3、AlCl3、MgCl2 、NH4Cl和 NaCl五种物质的溶液,这种试剂是A
A. 氢氧化钠溶液 B.盐酸 C. 氨水 D.硫氰化铵溶液
9.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即可构成CH4燃料电池。已知通入CH4的一极,其电极反应式是:CH4+10OH--8e-= CO32-+7H2O;通入O2的另一极,其电极反应式是:O2+2H2O+4e-= 4OH-,该电池放电时,下列有关叙述中,不正确的是( )
A.通入CH4的电极为负极 B.正极发生氧化反应
C.燃料电池工作时溶液中的阴离子向负极移动 D.该电池使用一段时间后应补充KOH
8. 有一种酸式盐AHB,它的水溶液呈弱碱性。今有下列几种说法,其中有错误的是( )
①相同的物质的量浓度的AOH溶液和H2B溶液,前者电离程度大于后者的电离程度;
②H2B不是强酸;
③HB-的电离程度大于HB-的水解程度;
④该盐在溶液中的电离方程式一般写成: AHB=A++HB- HB-=H++B2+
A.①② B.③④ C.②③ D.①④
7. 某学生设计了如图所示的方法,鉴定盐A的组成成分,由此分析,下列结论中,正确的是( )
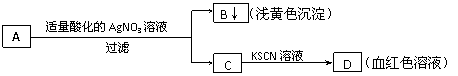
A.A中一定有Fe3+ B.C中一定有Fe3+
C.B为AgI沉淀 D.A一定为FeBr2溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com