
题目列表(包括答案和解析)
17.水的电离平衡如图所示:


(1)若A点表示25℃时水的电离平衡状态,当温度上升到100℃时,水的电离平衡状态到达B点。则此时水的离子积从_____增加到_____。
(2)将100℃时pH=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃时的恒温,于是混合物溶液的pH=7,则Ba(OH)2与盐酸溶液的体积比______
(3)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH与强碱的pH之间应满足的关系是

16.有甲、乙两个容积相等的恒容密闭容器,向甲中通入6mol A和2mol B,向乙中通入1.5mol
A、0.5mol B和3molC和2molD,将两容器的温度恒定在770K,使反应3A(g)+B(g) xC(g) +D(s)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题:
xC(g) +D(s)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题:
(1)若平衡时,甲、乙两容器中A的物质的量相等,则x=_________;若平衡时,甲、乙两容器中A的物质的量不相等,则x=_________。
(2)平衡时甲、乙两容器中A、B的物质的量之比是否相等____________(填“相等”或“不相等”),平衡时甲中A的体积分数为____________。
(3)若平衡时,甲、乙两容器中A的物质的量相等,改为按不同配比作为乙的起始物质,
达到平衡后,C的体积分数都仍为0.2。
①反应从逆反应方向开始,则D的起始物质的量应满足的条件是

②若加入0.6molA和0.2molB,则C和D起始物质的量分别应满足
,

(4)若平衡时两容器中的压强不相等,则两容器中压强之比为 : 。

15.向含有NH4+、Mg2+、Fe2+和Al3+的溶液中加入足量Na2O2微热并搅拌后,再加入过量
稀盐酸,溶液中大量减少的离子是 ( )
A.NH4+ B.NH4+、Fe2+

C.Al3+、Mg2+ D.Al3+

第Ⅱ卷(55分)
14. 在溶有Fe2(SO4)3和CuSO4的溶液中加入锌粉, 下列说法中不正确的是 ( )
在溶有Fe2(SO4)3和CuSO4的溶液中加入锌粉, 下列说法中不正确的是 ( )
A.若锌粉有剩余, 则不溶物中一定有铜,可能有铁
B.若锌粉有剩余, 则溶液中的金属阳离子只有Zn2+
C.若锌粉无剩余, 且溶液中尚存有Cu2+, 则一定有Fe2+
D.若锌粉无剩余, 且溶液中无Cu2+,则一定有Zn2+,一定无Fe3+,但不能确定有无Fe2+
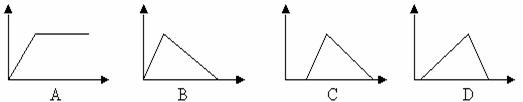
13.向盐酸和氯化铝的混合液中不断滴加氢氧化钠溶液,下列图象中, 能正确表示上述反应的是(横坐标表示加入氢氧化钠溶液的体积, 纵坐标表示反应生成沉淀的质量) ( )
12.把ag铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为ag,则原合金中铁的质量分数为 ( )
A.30% B.47.6% C.52.4% D.70%
11. 有一种锂电池,它是用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S。下列有关叙述中,正确的是 ( )
有一种锂电池,它是用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S。下列有关叙述中,正确的是 ( )
A.金属锂作电池的正极,石墨作电池的负极
B.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
C.电解质溶液中混入水,对电池反应无影响
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1
10.有甲、乙两种醋酸稀溶液,测得甲的pH=2,乙的pH=3。下列推断中正确的是( )
A.醋酸的物质的量浓度c(甲)=10c(乙)
B.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍
C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)=10V(甲)
D.甲中的c(OH-)为乙中c(OH-)的10倍
9.将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是 ( )
A.①③⑤⑦⑧ B.①⑥
 C.②④⑥⑧ D.②④⑦
C.②④⑥⑧ D.②④⑦
8.将pH=3的强酸溶液和pH=12的强碱溶液混合,当混合液的pH等于11时,强酸与强碱溶液的体积比是: ( )
A.10∶1 B.1∶9 C.9∶2 D.9∶1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com