
题目列表(包括答案和解析)
17. 在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)
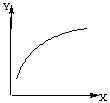
在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g) 2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
|
|
X |
Y |
|
A |
再加入A |
B的转化率 |
|
B |
再加入C |
A的体积分数 |
|
C |
增大压强 |
A的转化率 |
|
D |
升高温度 |
混合气体平均摩尔质量 |
16.右图曲线a表示放热反应X(g)+Y(g) 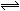 Z(g)+M(g)+N(g)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应的过程按b曲线进行,可采取的措施是
Z(g)+M(g)+N(g)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应的过程按b曲线进行,可采取的措施是
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
15.以下反应可以用熵判据来解释的是
A.硝酸铵自发地溶于水
B.CaO(s)+CO2(g)==CaCO3(s) △H=-175.7kJ/mol
C.(NH4)2CO3(s)==NH4HCO3(s)+NH3(g) △H=+74.9kJ/mol
 D.2H2(g)+O2(g)==2H2O(l) △H=-285.8kJ/mol
D.2H2(g)+O2(g)==2H2O(l) △H=-285.8kJ/mol
14.下列反应中,生成物的总能量小于反应物总能量的是
A、Ba(OH)2.8H2O与NH4Cl(固体)的反应 B、铁生锈
C、碳在氧气中燃烧 D、焦碳在高温下与水蒸气反应
13.给蒸馏水中滴入少量盐酸后,下列说法中错误的是
A.[H+ ][OH- ]乘积不变 B.pH增大了
C.[OH- ]降低了 D.水电离出的[H+ ]增加了
12.下列物质的水溶液中,除水分子外,不存在其它分子的是
A.NaCl B.KHSO4 C.CH3COOH D.HClO
11.已知400℃和1.01×105Pa时的气体摩尔体积为55.20L·mol-1,在该条件下有1mol气体X发生如下反应并达到平衡:2X(g) mY(g) +Z(g),测得平衡混合气体中X的体积分数为58.80%,混合气体的总质量为46.00g,混合气体的密度为0.72g·L-1。则平衡混合气体的平均相对分子质量为
A.58.80 B.46.00 C.39.74
D.16.13
mY(g) +Z(g),测得平衡混合气体中X的体积分数为58.80%,混合气体的总质量为46.00g,混合气体的密度为0.72g·L-1。则平衡混合气体的平均相对分子质量为
A.58.80 B.46.00 C.39.74
D.16.13
10. 在密闭容器中,对于反应:2SO2(g)+O2(g)  2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为
2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为
A.10 mol和10% B.20 mol和20%
C.20 mol和40% D.20 mol和80%
9.恒温恒压下,在容积可变的器皿中,反应2NO2(g) N2O4(g) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4(g) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.不变 B.增大 C.减小 D.无法判断
8.某温度下,在容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为6mol、3mol和6mol。保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是
A.均减半 B.均加倍 C.均增加2mol D.均减少2mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com