
题目列表(包括答案和解析)
9.下列有关电化学知识的描述中正确的是( )
A.原电池的正极和电解池的阳极均发生氧化反应
B.氢燃料电池把氢气在氧气中燃烧放出的热能转化为电能
C.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)耐腐蚀
D.铅蓄电池充电时电源的正极接蓄电池标“-”的一极
8.下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用铜片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面出现一层铜
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把铁片敢入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
7.
 对于2SO2+O2 2S03,△H<O的反应,下列说法中正确的是( )
对于2SO2+O2 2S03,△H<O的反应,下列说法中正确的是( )
A.当SO2和SO3的浓度相等时,反应达到化学平衡状态
B.当生成SO:的速率与生成SO,的速率相等时,反应达到化学平衡状态
C.温度一定,若SO2、O2、SO3的起始浓度不同,反应达到平衡时,SO3的平衡浓度一定也不同
D.只有当外界条件改变,使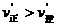 ,才能引起上述化学反应的平衡状态发生移动
,才能引起上述化学反应的平衡状态发生移动
6.


 设C+CO2 2C0(吸热反应)反应速率为v1,N2+3H2 2NH3(放热反应)反应速率为v2。对于上述反应,升高温度时, v1和v2的变化情况为( )
设C+CO2 2C0(吸热反应)反应速率为v1,N2+3H2 2NH3(放热反应)反应速率为v2。对于上述反应,升高温度时, v1和v2的变化情况为( )
A.都增大 B.都减小
C.v1增大,v2减小 D.v1减小,v2增大
5.下列描述中,不符合生产实际的是( )
A.合成氨工业中,N2和H2的最佳配比应为物质的量之比1:3
B.电解法精炼粗铜,用纯铜作阴极
C.工业上电解饱和食盐水制烧碱,用离子交换膜阻止0H-移向阳极
D.在镀件上电镀锌,锌作阳极
4.如图所示,下列叙述不正确的是( )
A.该装置是原电池
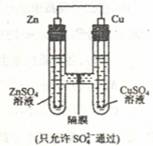 B.锌为负极,发生氧化反应
B.锌为负极,发生氧化反应
C.硫酸根离子从左流向右
D.铜棒的质量会增重
3.
 可逆反应A+3B 2C+2D,在四种不同的情况下的反应速率分别为( )
可逆反应A+3B 2C+2D,在四种不同的情况下的反应速率分别为( )
①v(A)=0.15 mol·L-1·S-1②v(B)=O.6 mol·L-1·S-1③v(C)=0.4 mol·L-1·S-1
④v(D)=O.45 mol·L-1·S-1。该反应进行最快的是( )
A.① B.②和③ C.④ D.①和④
2.据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极主要发生的反应是( )
A.2H++2e-=H2↑ B.2H20+02+4e-=40H-
C.Fe-2e-=Fe2+ D.40H--4e-=2H20+02↑
1.下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.新键生成时释放的总能量大于旧键断裂时吸收的总能量时,反应为吸热反应
C.反应产物的总焓大于反应物的总焓时,反应吸热,△H>O
D.△H的大小与热化学方程式的计量系数无关
25.(14分)味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”。某学校化学科研小组现对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:资料表明谷氨酸钠的存在不影响NaCl含量进行测定。
Ⅱ.设计实验方案:
(1)实验原理:____________________________________________________________。
(2)实验试剂:水、试剂X的溶液等
(3)实验过程:
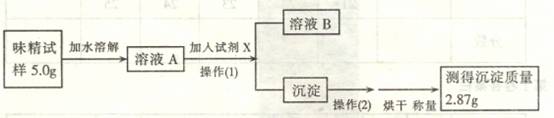
根据上述实验步骤回答下列有关问题:
①操作(1)所需要的玻璃仪器有_____________________________________________。
②操作(2)的名称为______________________________________。
③通过计算判断该味精中NaCl的质量分数,是否符合其包装上标注的标准。
④若溶液A的体积为100 mL,则溶液A中NaCl的物质的量浓度是多少?(第③④问
写出必要的计算过程)
2008--2009学年度第一学期学段检测
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com