
题目列表(包括答案和解析)
8.某同学在所收到的信封上发现有收藏价值的邮票,便将邮票剪下来浸入水中,以去掉邮票背面的黏合剂。根据“相似相溶”原理,该黏合剂的成分可能是
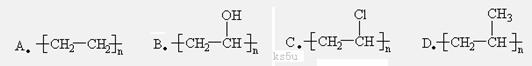
7.盐酸洛派丁胺俗称易蒙停,它是一种新型的止泻药,适用于各种急慢性腹泻的治疗,其结构简式如图:下列说法正确的是
 A.易蒙停的分子式为C29H33Cl2N2O3
A.易蒙停的分子式为C29H33Cl2N2O3
B.向易蒙停溶液中加入FeCl3溶液,溶液
显紫色
C.1mol易蒙停只能与lmolNaOH发生反应
D.lmol易蒙停最多能与3mol溴水发生反应
6.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是
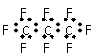 A.分子中三个碳原子可能处于同一直线上
A.分子中三个碳原子可能处于同一直线上
B.全氟丙烷的电子式为:
C.相同压强下,沸点:C3F8<C3H8
D.全氟丙烷分子中既有极性键又有非极性键
5. 2008年9月11日,有媒体报道,甘肃14名婴儿患肾结石,省卫生厅介入调查,初步认为可能与某品牌奶粉有关。随后,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉收到三聚氰胺污染,并宣布召回市面上被污染的产品。质检总局,卫生部等有关部门随即展开调查。三聚氰胺的分子结构如下:
2008年9月11日,有媒体报道,甘肃14名婴儿患肾结石,省卫生厅介入调查,初步认为可能与某品牌奶粉有关。随后,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉收到三聚氰胺污染,并宣布召回市面上被污染的产品。质检总局,卫生部等有关部门随即展开调查。三聚氰胺的分子结构如下:
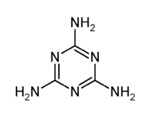
有关三聚氰胺的说法正确的是
A.三聚氰胺属于芳香族化合物,但不属于芳香烃
B.三聚氰胺的分子式为C3N6H6
C.三聚氰胺中的碳原子属于饱和碳原子
D.三聚氰胺分子中的所有原子都在一个平面内
4.下列除去括号内杂质的有关操作方法不正确的是
A.乙烷(乙炔):通过盛溴水的洗气瓶
B.乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热
C.苯(苯酚):加入氢氧化钠溶液,然后分液
D.乙醇(水):加入生石灰,然后蒸馏
3.下列关于乙烯和聚乙烯的叙述中正确的是:
A.二者都能使溴的四氯化碳溶液褪色 B.二者互为同系物
C.二者实验式相同 D.聚乙烯是乙烯的缩聚产物
2.在下列实验中,应将温度计插入水浴中的是: A. 在实验室中蒸馏石油 B.由苯制硝基苯 C.由酒精制乙烯 D.由乙酸与乙醇反应制乙酸乙酯
1.2008年北京奥运会火炬以中国传统祥云符号和纸卷轴为创意,由铝合金制成,使用的燃料为丙烷。下列说法不正确的是
A.丙烷与甲烷互为同系物 B.通常条件下,丙烷性质稳定,不与酸、碱和氧化剂发生反应
C.丙烷燃烧是吸热反应
D.火炬燃料用丙烷比用煤油更环保
21.(12分)在一定温度下,在一体积固定的密闭中加入2 mol X和1 mol Y,发生如下反应:

 2X(g)+Y(g) a Z(g)+W(g) △H=-Q kJ·mol-1(Q>O)(a是正整数)当反应达到平衡后,反应放出的热量为Q1kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
2X(g)+Y(g) a Z(g)+W(g) △H=-Q kJ·mol-1(Q>O)(a是正整数)当反应达到平衡后,反应放出的热量为Q1kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值_______________(填“增大”、“减小”或“不变”)。
(2)化学计量数a的值为______________。
(3)有同学认为,Q1一定小于Q,你认为该结论是否正确?___________________,其理由是____________________________________________________________。
(4)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是_____________(稀有气体不参与反应)。
A.2 molX、1mol Y、1molAr
B.a molZ、1mol W
C.1 molX、0.5mol Y、0.5a molZ、O.5 mol W
D.2 molX、1mol Y、lmolZ
(5)X的转化率α=_______________________(用含Q、Q1的代数式表示)。
2008-2009学年度第一学期学段检测
20.(12分)
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。

(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:

 CO2(g)+3H2(g) CH30H(g)+H20(g)△H=-49.0kJ·mol-1测得C02和CH3OH(g)的浓度随时间变化如上图所示。
CO2(g)+3H2(g) CH30H(g)+H20(g)△H=-49.0kJ·mol-1测得C02和CH3OH(g)的浓度随时间变化如上图所示。
①从反应开始到平衡,以氢气表示的平均反应速率v(H2)=____________mol·L-1·min-1。
②下列措施中能使n(CH3OH)/n(C02)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入lmol CO2和3mol H2
(2)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的02,科研工作者通过某种电化学装置实现了上述目的。该电化学装置内的总反应为:2CO2=2CO+O2,阴极反应式为:2C02+4e-+2H20=2C0+40H-,则阳极反应为:___________________________。该反应产生的CO会对环境产生污染,有人提出,通过加强热使CO分解的方法来消除污染,请你判断是否可行?________,说出理由:____________________________________________。 (已知反应2C0=2C+O2的△H>O、△S<O)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com