
题目列表(包括答案和解析)
5. 在10mL0.1mol/L的醋酸中逐滴加入0.1mol/L的氢氧化钠溶液,当滴至混合液恰好呈中性时,消耗氢氧化钠溶液的体积( )
A、等于10mL B、小于10mL C、大于10mL D、无法判断
4. 下列金属制的器皿可以用来放置冷的浓硫酸的是( )
A、铁 B、镁 C、钠 D、锌
3. 下列各组离子中,在溶液中不能大量共存的是( )
A、S2-、NO3-、CO32-、K+ B、Al3+、Na+、H+、SO42-
C、H+、NH4+、K+、SO42- D、Fe2+、Ca2+、OH-、NO3-
2. 铁原子的最外层电子数是( )
A、1 B、2 C、2或3 D、3
1. 下列溶液中,呈酸性的是( )
A、硫酸钠溶液 B、碳酸钠溶液 C、氯化钠溶液 D、氯化铵溶液
22. (8分)分子组成符合CnH2n-2的某烃,分子结构中无支链和侧链。完全燃烧时所消耗的氧气的体积是相同状况下该烃蒸气体积的8.5倍。
(1)求该烃的分子式
(2)若该烃为链状烯烃,且与等物质的量的Br2加成后只能得到单一的产物,试推断并写出其结构简式:
(3)若该烃只能与等物质的量的Br2发生加成反应,试写出其结构简式。
21.( 10分)X、Y是中学化学里常用的物质,其中Y是单质,X是化合物;它们之间相互反应以及生成物之间的关系如下图所示:
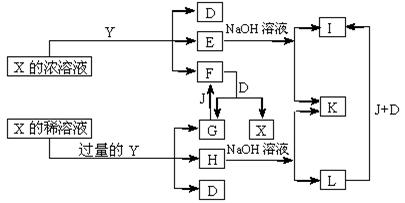
已知E溶液跟NH4SCN的稀溶液混合时,溶液呈血红色。请回答:
(1)Y和X浓溶液反应的条件是 ,而常温下难反应的原因是 。
(2)写出F和G相互转化的化学方程式:
F→G+X G→F
(3)L转化成I的现象是 ,有关的化学方程式是 。
20.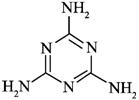 (9分)三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”。三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃。三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺。与该法相比,尿素法成本低,目前较多采用。尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6
CO(NH2)2 → C3N6H6
+ 6 NH3 + 3 CO2
(9分)三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”。三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃。三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺。与该法相比,尿素法成本低,目前较多采用。尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6
CO(NH2)2 → C3N6H6
+ 6 NH3 + 3 CO2
试回答下列问题:
(1)原子数和电子总数都相等的粒子互称为等电子体,它们具有相似的结构特征,与CN22-互为等电子体的中性分子有N2O和 (填化学式),由此可以推知CN22-离子的空间构型为 ;
(2)写出由电石和N2在加热条件下反应制备氰胺化钙的化学方程式:
;
若通过上述反应制备400g氰胺化钙,则转移的电子数为 mol;
(3)三聚氰胺难溶于冷水但易溶于热水,以尿素为原料制得的三聚氰胺粗产品中既含有不溶于水的杂质,又含有易溶于水的杂质,简述从粗产品中提纯三聚氰胺的方法:
(4)在奶粉中掺入三聚氰胺后不易被发现的原因是
19.(8分)在化工生产中,要用到一种无色、可溶于水的晶体:铝铵矾。该晶体是一种复盐,其主要成分是十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化。已知NH4+和AlO2-在水溶液中不能大量共存:
NH4+ + AlO2-+H2O=Al(OH)3↓+NH3↑
试回答:(1)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少。
请答出各种现象由先到后出现的顺序(用序号回答)____→____→____→____→____;
 (2)写出滴入NaOH溶液的过程中,有关反应的离子方程式:
(2)写出滴入NaOH溶液的过程中,有关反应的离子方程式:
①__ __
②_ _;
③__ __。
18.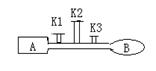 (8分)A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。
(8分)A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。
(已知:2NO2  N2O4;△H<0)
N2O4;△H<0)
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA_________VB。(填“>”、“<”、“=”);若打开活塞K2,气球B将__________(填:变大、变小、不变)。
(2)若在A、B中再充人与初始量相等的NO2,则达到平衡时,NO2的转化率αA将_________ (填增大或减小、不变);若通人等量的Ne气,则达到平衡时,A中NO2的转化率将_________,B中NO2的转化率将_________(填:变大、变小、不变)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,_________中的颜色较深。
(4)若在容器A中充人4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com