
题目列表(包括答案和解析)
20. 右图为阳离子交换膜法电解饱和食盐水原理示意图。 下列说法不正确的是 A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,
精制时先加Na2CO3溶液
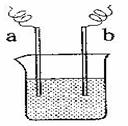
19、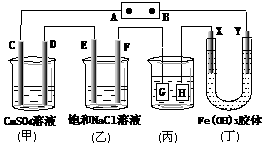 如下图所示的装置,C、D、E、F、X、Y都是惰
如下图所示的装置,C、D、E、F、X、Y都是惰
性电极。将电源接通后,向(乙)中滴入酚酞溶液,在
F极附近显红色。则以下说法正确的是
A.电源B极是正极
B.(甲)、(乙)装置的C、D、E、F电极均有单质生
成,其物质的量比为1∶2∶2∶2
C.欲用(丙)装置给铜镀银,G应该是Ag,电镀液
选是AgNO3溶液
D.装置(丁)中X极附近红褐色变浅,说明氢氧化铁胶粒带负电荷
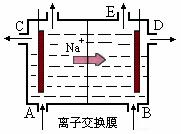
18、相同条件下,下列装置中指定电极的电极反应式相同的是
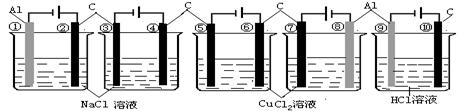
A.②④⑥⑦⑩ B.①③⑤⑧⑨ C.②③④⑤⑥⑦⑩ D.①③⑤⑦⑨
17、在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g);△H=-566kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-890kJ·mol-1
又知由H2与O2反应生成液态H2O 比生成气态H2O 多放出44kJ/mol的热量。则CH4 气体在空气中不完全燃烧热化学方程式正确的是
A.2CH4(g)+O2(g) CO2(g)+CO(g)+4H2O(1)△H=-1214kJ·mol-1
B.2CH4(g)+O2(g) CO2(g)+CO(g)+4H2O(g)△H=-1038kJ·mol-1
C.3CH4(g)+5O2(g) CO2(g)+2CO(g)+6H2O(1) △H=-1538kJ·mol-1
D.3CH4(g)+5O2(g) CO2(g)+2CO(g)+6H2O(g) △H=-1840kJ·mol-1
16、在1 L密闭容器中,把1 mol A和1
mol B混合发生如下反应:3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4
mol/L,下列叙述中不正确的是( )
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4
mol/L,下列叙述中不正确的是( )
A.x的值为2 B.A的转化率为40%
C.B的平衡浓度为0.8 mol/L D.D的体积分数为25%
15、 据媒体报道:以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢为燃料,空气为氧化剂,铂做催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是
①正极反应为:O2 + 4H+ + 4e- = 2H2O ②负极反应为:2H2-4e- = 4H+
|
③总的化学反应为:2H2 + O2 === 2H2O ④氢离子通过电解质向正极移动 (A)①②③ (B)②③④ (C)①②④ (D)①②③④
14、一定量的A、B混合气体在密闭容器中发生如下反应:mA(g)+nB(g) pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/2,当达到新的平衡时,C的浓度为原来的1.8倍,则下列说法正确的是
pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/2,当达到新的平衡时,C的浓度为原来的1.8倍,则下列说法正确的是
A、m+n>p B、A的转化率降低
C、平衡向正反应方向移动 D、C的体积分数减小
13、在电子表里使用的纽扣电池,其电极材料分别是Zn和Ag2O,
电解质溶液是KOH溶液。电池工作时的电极反应式分别为:
Ag2O+2e+H2O=2Ag+2OH-
Zn-2e+2OH-=ZnO+H2O
下列说法正确的是:
A.Ag2O是电池的正极,Zn是电池的负极
B.Zn 是电池的正极,Ag2O 是电池的负极
C.电池工作时,电池负极区溶液的OH-的浓度增大
D.电池工作时,电池负极区溶液的OH-的浓度减小
12、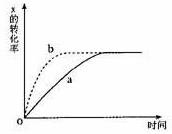 右图曲线a表示放热反应 X(g)+Y(g)
右图曲线a表示放热反应 X(g)+Y(g) 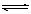 Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是 ( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是 ( )
A.升高温度
B.加大X的投入量
C.加催化剂
D.增大压强
10、一处于化学平衡状态的反应X(s)+3Y(g) 2Z(g)(正反应为放热反应)。为了使化学平衡向生成Z的方向移动,应选择的条件是
2Z(g)(正反应为放热反应)。为了使化学平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加入催化剂⑥分离出Z ⑦增大X的浓度
A.①③⑤⑦ B.②③⑤⑦ C.②③⑥ D.②④⑥
11一定条件下,反应2HI(g) H2(g)+I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是①增大H2的浓度;②升高温度;③降低温度;④缩小体积; ⑤增大HI的浓度;⑥减小压强
H2(g)+I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是①增大H2的浓度;②升高温度;③降低温度;④缩小体积; ⑤增大HI的浓度;⑥减小压强
A、①③⑥ B、③⑤⑥ C、①③⑤ D、②④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com