
题目列表(包括答案和解析)
22、(7分)2SO2(g)+O2(g)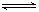 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol
SO3的ΔH= -99kJ·mol-1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol
SO3的ΔH= -99kJ·mol-1.请回答下列问题:
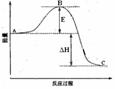 (1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol-1;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H为
21、(8分)如果改变影响平衡的一个条件(如 、 或 等),平衡就向 方向移动,这就是平衡移动原理,也叫 。
催化剂对化学平衡状态 影响(“有”或“无”),原因是 。
20.将1体积A气体和3体积B气体混合,发生如下反应并达到平衡:2A(g) + B(g) 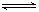 2C(g),在同温同压下测得在反应前后混合气体的密度之比为9∶10,则A的转化率为
2C(g),在同温同压下测得在反应前后混合气体的密度之比为9∶10,则A的转化率为
A.90% B.80% C.45% D.10%
太 原 五 中
2009-2010年学年度第一学期月考(10月)
高二化学(理)答卷纸
满分为100分,考试用时90分钟
19. 已知:Fe2O3(s)+3/2 C(s)= 3/2 CO2(g)+2Fe(s) △H=234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
则2Fe(s)+3/2 O2(g)=Fe2O3(s)的△H是
A.-824.4kJ·mol B.-627.6kJ·mol-1
C.-744.7kJ·mol-1 D.-169.4kJ·mol-1
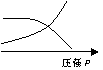
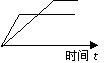
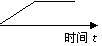
17、如图是表示:2X(g)+Y(g) 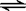 Z(g)+R(s)+Q(g)的 v
Z(g)+R(s)+Q(g)的 v
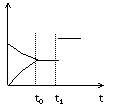
气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,
则所改变的条件符合曲线的是
A.减少Z物质 B.加大压强
C.升高温度 D.使用催化剂
|
|
|
|
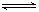 2C(g) △H<0,下列各图中正确的是
2C(g) △H<0,下列各图中正确的是
|
|
|
|



|
|
|
|
|
|
|
|
16、把NO2气体装入带活塞的圆筒中慢慢压缩,体积增大到原来的2倍。下列叙述正确的是
 A、平衡不移动,压强为原来二倍 B、平衡移动,NO2浓度减小
A、平衡不移动,压强为原来二倍 B、平衡移动,NO2浓度减小
C、平衡不移动,N2O4的百分含量增大1倍
D、平衡移动,压强增大,但小于原来的2倍
15、将 4 mol A
气体和 2 mol B
气体在 2 L 的容器中混合并在一定条件下发生如下反应2A(气)+B(气)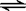 2C(气)若经2s后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为70%
④ 2 s 时物质 B 的浓度为 0.7 mol·L-1,其中正确的是
2C(气)若经2s后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为70%
④ 2 s 时物质 B 的浓度为 0.7 mol·L-1,其中正确的是
A.①③ B. ①④ C. ②③ D. ③④
14.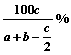 在合成氨的反应中,由a mol N2和b mol H2混合反应达到平衡平衡时有c mol NH3生成,则NH3在反应混合物中所占的体积分数是
在合成氨的反应中,由a mol N2和b mol H2混合反应达到平衡平衡时有c mol NH3生成,则NH3在反应混合物中所占的体积分数是
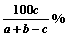
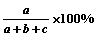
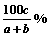 A. B.
C.
D.
A. B.
C.
D.
13、在一密闭烧瓶中注入NO2,在25℃时建立下列平衡:2NO2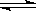 N2O4
ΔH <0,若把烧瓶置于100℃的沸水中,下列情况中①颜色,②平均摩尔质量,③质量,④压强,⑤密度,保持不变的是(
)。
N2O4
ΔH <0,若把烧瓶置于100℃的沸水中,下列情况中①颜色,②平均摩尔质量,③质量,④压强,⑤密度,保持不变的是(
)。
A. ③⑤ B. ③④ C. ②④ D. ①③
12、可逆反应2SO2 (g)+
O2(g) 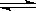 2SO3(g)达到平衡的标志是
2SO3(g)达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
A、①② B、①③ C、只有③ D、只有①
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com