
题目列表(包括答案和解析)
8.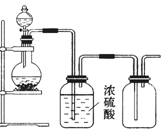 可用图示装置制取(必要时可加热)、净化、收集的气体是
可用图示装置制取(必要时可加热)、净化、收集的气体是
A.铜和稀硝酸制一氧化氮
B.氯化钠与浓硫酸制氯化氢
C.锌和稀硫酸制氢气
D.硫化亚铁与稀硫酸制硫化氢
6.铜粉放入稀H2SO4中,加热后无明显现象,当加入一种盐后,铜的质量减小,溶液变蓝,同时有气体逸出,此盐可能是
A.FeSO4 B.Na2CO3 C.KNO3 D.KCl
7.做实验时不小心沾了一些高锰酸钾,皮肤上的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO4-+C2O42-+H+→CO2↑+Mn2+ +
关于此反应的叙述正确的是:
A.该反应的氧化剂是C2O42- B.该反应右边方框内的产物是OH-
C.该反应电子转移总数是5e- D.配平该反应后,H+的化学计量数是16
5.阿波罗宇宙飞船升入太空是以N2H4(联氨)和N2O4为推力源。反应温度高达2700℃,反应式为2N2H4+N2O4==3N2+4H2O。对于该反应的说法正确的是
A.联氨是氧化剂 B.氧化产物和还原产物的质量比为1∶2
C.属于置换反应 D.联氨是还原剂
4.下列试剂:①浓氨水;②氯水;③硝酸银;④浓硝酸;⑤浓盐酸;⑥溴化银,其中必须用棕色试剂瓶保存的有
A.①②③④⑤⑥ B.②③④⑥ C.②③⑤⑥ D.①③④⑥
3.碱石灰和五氧化二磷均能干燥的一组气体是
A.N2、O2、NH3 B.CO、NO、H2 C.H2、NO、NH3 D.NO、Cl2、N2
2. 将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)
2C(g)。若经2 s后测得C的溶液为0.6mol·L-1,现有下列几种说法;
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)
2C(g)。若经2 s后测得C的溶液为0.6mol·L-1,现有下列几种说法;
①物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率70%;
④2 s时物质B的浓度为0.7 mol·L-1。其中正确的是
A.①③ B.①④ C.②③ D.③④
1.X、Y、Z三种气体进行下列反应3X+Y==2Z,在三不同情况下测得速率值为:
 ①v(X) =1 mol·L-1·s-1;
①v(X) =1 mol·L-1·s-1;
②v(Y)=30 mol·L-1·min-1;
③v(Z)=0.5 mol·L-1·s-1,
这三种情况下,能正确比较反应的速率的是
A.③>②>① B.②>①>③ C.①>②>③ D.③>①>②
20.(16分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 ,
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
 永安一中2008-2009学年下学期第一次月考
永安一中2008-2009学年下学期第一次月考
19、(12分)氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。请回答下列问题。
(1)砷原子核外电子排布式为______________________________。(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为________________,该晶体的配位体为____________。
(3)已知:
|
|
CH4 |
SiH4 |
NH3 |
PH3 |
|
沸点(K) |
101.7 |
161.2 |
239.7 |
185.4 |
|
分解温度(K) |
873 |
773 |
1073 |
713.2 |
分析上表中四种物质的相关数据,请回答:
① CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是_________________________________________________________________________________________________。
② CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是___________________________________________________________________________________________________。
③综合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时__________先液化。
18、(各2分,共12分)Pt(NH3)2Cl2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
(1)Pt(NH3)2 Cl2是平面正方形结构,还是四面体结构
(2)请在以下空格内画出这两种固体分子的几何构型图,
淡黄色固体: , 黄绿色固体:
(3)淡黄色固体物质是由 分子组成,黄绿色固体物质是由
分子组成(填“极性分子”或“非极性分子”)
(4)黄绿色固体在水中溶解度比淡黄色固体大,原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com