
题目列表(包括答案和解析)
8.
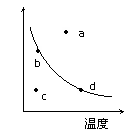 右图中的曲线表示的是其他条件一定时,反应:2NO+O2
右图中的曲线表示的是其他条件一定时,反应:2NO+O2 2NO2 DH<0中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是( )
2NO2 DH<0中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是( )
A.a点 B.b点
C.c点 D.d点
7. 对于任何一个化学平衡体系,采取以下措施,一定会使平衡发生移动的是( )
A.加入一种反应物 B.增大体系的压强
C.升高温度 D.使用催化剂
6. 已知在1.01×105Pa、298K条件下,2mol 氢气在氧气中燃烧生成水蒸气放出484kJ热量。下列热化学方程式正确的是( )
A.H2O(g)===H2(g)+O2(g) △H=+242kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l) △H=-484kJ·mol-1
C.H2(g)+O2(g)===H2O(g) △H=+242kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g) △H=+484kJ·mol-1
5. 下列能够使反应:Cu+2H2O==Cu(OH)2+H2↑获得成功的是( )
A.Cu与稀H2SO4发生反应
B.铜--锌合金在潮湿的空气中发生反应被腐蚀
C.用铜片作阴、阳电极,电解氯化钠溶液
D.用铜片作阴、阳电极,电解硫酸溶液
4. 用惰性电极实现电解,下列说法正确的是( )
A.电解稀硫酸,实质上是电解水,故溶液pH不变
B.电解稀NaOH溶液,要消耗OH-,故溶液pH减小
C.电解CuCl2溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
D.电解Na2SO4溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2
3. 用惰性电极电解AgNO3溶液一段时间后,下列有关说法正确的是( )
A.阳极质量增加
B.电解过程中溶液的pH不断升高
C.向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况
D.电解后两极产生的气体体积比为2∶1
2. 已知某反应的焓变小于零,则下列叙述正确的是( )
A.该反应一定是放热反应
B.该反应一定是吸热反应
C.该反应中反应物的总能量一定小于产物的总能量
D.该反应需要加热才能发生
1. 下列说法正确的是( )
A.需要加热的化学反应都是吸热反应
B.中和反应都是放热反应
C.原电池是将电能转化为化学能的一种装置
D.水力发电是将化学能转化为电能的过程
20.(8分)加热500g含(NH4)2SO413.2%的硫酸铵和碱石灰组成的混合物,并把生成的氨气氧化成NO,再继续氧化成NO2,最后全部转化成HNO3(反应过程中无损耗),求:
(1)反应共需标准状况下的氧气多少升?
(2)可制得多少克硝酸?
18. (18分)如图所示装置是某种气体X发生装置和收集装置(必要时可加热)。所用的试剂从下列试剂中选取2~3种;硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水。
(18分)如图所示装置是某种气体X发生装置和收集装置(必要时可加热)。所用的试剂从下列试剂中选取2~3种;硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水。
请回答下列问题:
(1)气体X的化学式是_________________。
(2)所选药品a是__________,b是______________,c是______________,装置B的作用是______________________________。
(3)用所选的药品发生反应生成X时,离子方程式是_______________________________ (4)在反应开始后A中的主要现象是:①_______________________________________,
②________________________________,③___________________________________。
|
NH4HCO3+Ca(OH)2===CaCO3+NH3↑+2H2O↑
|
NH4HCO3===NH3↑+CO2↑+H2O↑
取碳酸氢铵和熟石灰的混合物共0.1mol,在密闭容器中加热至200℃,充分反应后,排出多余的气体,冷却后称量,固体剩余物质量为ag。
(1)碳酸氢铵和熟石灰以等物质的量混合时,a=______________。
(2)若以b mol表示混合物中碳酸氢铵的物质的量,通过计算确定a随b变化的数学表达式。
当0<b≤0.05时,a=__________________
当0.05<b<0.1时,a=_________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com