
题目列表(包括答案和解析)
23.在一定条件下,可逆反应:mA+nB pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是 。
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是 。
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)
21. 在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系.
Cr2O72-+H2O 2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈___________色,因为__________。
2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈___________色,因为 __________。22. 在一固定容积的密闭容器中,保持一定条件下进行以下反应:
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈___________色,因为__________。
2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈___________色,因为 __________。22. 在一固定容积的密闭容器中,保持一定条件下进行以下反应:
X(气)+2Y(气) 3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为 mol。
(2)在相同实验条件下,若在同一容器中改为加入2 mol X和8 mol Y,若要求在反应混合气体中Z体积分数不变,则还需加入Z mol。并写上述反应的平衡常数表达式 。
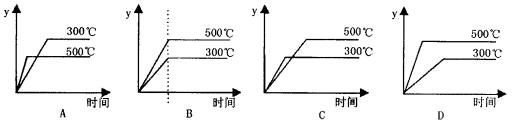
20. 对于热化学方程式:SO3(g)  SO2(g)+
1/2 O2(g) ;△H=+ 98.3kJ•mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)
( )
SO2(g)+
1/2 O2(g) ;△H=+ 98.3kJ•mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)
( )
第Ⅱ卷(非选择题)
19. 在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应:A(S)+3B(g)
 2C(g)+D(g)
已达平衡状态的是
( )
A 混合气体的压强不随时间变化 B B的生成速率和D的反应反应速率为3:1
C 混合气体的密度不随时间变化 D B、C、D的分子数之比为3:2:1
2C(g)+D(g)
已达平衡状态的是
( )
A 混合气体的压强不随时间变化 B B的生成速率和D的反应反应速率为3:1
C 混合气体的密度不随时间变化 D B、C、D的分子数之比为3:2:1
18. 下图表示的平衡混和物中,产物X的百分含量在不同压力下随温度改变的情况,在下述哪一个可逆体系中X可代表用横线标明的物质
( )
A N2(g)+O2(g) 2NO(g)(正反应吸热)
B 2SO3(g)
2NO(g)(正反应吸热)
B 2SO3(g) 2SO2(g)+O2(g)(正反应吸热)
C N2(g)+3H2(g)
2SO2(g)+O2(g)(正反应吸热)
C N2(g)+3H2(g)  2NH3(g)(正反应放热)
D 4NH3(g)+3O2(g)
2NH3(g)(正反应放热)
D 4NH3(g)+3O2(g)  2N2(g)+6H2O(g)(正反应放热)
2N2(g)+6H2O(g)(正反应放热)

17. 将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应2A(g)+B(g)==2C(g),v 若经2s(秒)后测得C的浓度为0.6mol·L-1,现有下列几种说法: ①用物质A表示的反应的平均速率为0.3mol·L-1·s-1;②用物质B表示的反应的平均速率为0.6mo1.L-1·s-1;③2s时物质A的转化率为70%;④2s时物质B的浓度为0.7mol·L-1其中正确的是 ( ) A.①③ B.①④ C.②③ D.③④
16. 在一密闭烧瓶中,在25℃时存在着平衡:2NO2  N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
( )
①颜色 ②平均分子量 ③质量 ④压强
⑤密度
A ①和③ B ②和④
C ④和⑤ D ③和⑤
N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
( )
①颜色 ②平均分子量 ③质量 ④压强
⑤密度
A ①和③ B ②和④
C ④和⑤ D ③和⑤
15. 在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用v(A)、v(B)、
v(C)(mol·L-1·s-1)表示且v(A)、v(B)、v(C)之间有以下关系:v(B)=3v(A),3v(C)=2v(B)。则此反应可表示为
( )
A.2A+3B  2C B.A+3B
2C B.A+3B  2C
C.3A+B
2C
C.3A+B  2C D.A+B
2C D.A+B  C
C
14. 在373 K时,把0.5 mol N2O4通入体积为5 L的真空密闭容器中,立即出现棕色。反应进行到2 s时,NO2的浓度为0.02 mol·L-1。在60 s时,体系已达平衡,此时容器内压强为开始的1.6倍。 下列说法正确的是 ( ) A. 前2 s,以N2O4的浓度表示的平衡反应速率为0. 01 mol·L-1·s-1
B. 在2 s时体系内的压强为开始时的1. 1倍
C. 在平衡时体系内含N2O4 0. 25 mol
D. 平衡时,如果压缩容器体积,则可提高N2O4的转化率
13. 对已达到平衡的反应:2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
2Z(g),减小压强时,对反应产生的影响是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com