
题目列表(包括答案和解析)
8. 下列有关能量转换的说法正确的是
(
)
下列有关能量转换的说法正确的是
(
)
A.煤燃烧是化学能转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
7. 已知:H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol, 则反应2HCl(g)= H2(g)+ Cl2(g)的△H为( )
A.+184.6 kJ/mol B.-92.3 kJ/mol C.-369.2 kJ/mol D.+92.3 kJ/mol
6. m A
+ n B 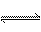 p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为 ( )
p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为 ( )
A、2:3:2 B、2:3:3 C、1:3:2 D、3:1:2
5.氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:H2(g) + 1/2O2(g) = H2O(l);△H= -285.8 kJ/mol
CO(g) + 1/2O2(g) = CO2(g);△H= -283.0 kJ/mol
C8H18(l) + 25/2O2(g) = 8CO2(g) + 9 H2O(l);△H= -5518 kJ/mol
CH4(g) + 2 O2(g) = CO2(g) + 2 H2O(l);△H= -890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是( )
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
4.已知:H2(g)+F2(g) = 2HF(g) ;ΔH=-270 kJ/mol,下列说法正确的是
A.2L氟化氢气体分解成1L氢气与1L氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量小于270kJ热量
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270kJ热量
3.已知Zn(s)+1/2O2(g)=ZnO(s);ΔH=-350 kJ/mol,则1 mol Zn在氧气中燃烧放出的热量约为 ( )
A.5.4 kJ B.350 KJ C.3.5 kJ D.8.5 Kj
2.已知下列热化学方程式:
2H2(g)+O2(g)=2H2O(g); ΔH=-483.6 kJ/mol
H2(g)+1/2O2(g)=H2O(g); ΔH=-241.8 kJ/mol
H2(g)+1/2O2(g)=H2O(l); ΔH=-285.8 kJ/mol
则氢气的燃烧热ΔH为 ( )
A.-438.6 kJ/mol B.-241.8 kJ/mol
C.-285.8 kJ/mol D.无法确定
1.下列反应中生成物总能量高于反应物总能量的是 ( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
22. 为测定淀粉水解的百分率,称取100g直链淀粉溶于水,实验步骤如下:
为测定淀粉水解的百分率,称取100g直链淀粉溶于水,实验步骤如下:
淀粉溶液 混合液
①所加试剂名称A , C_________________.
②只加A,不加B是否可以________,理由是:____________________________________.
③在足是C的作用下,析出金属单质 2.16g,淀粉的水解率是 2009-2010学年度高二年级上学期第一次月考
21.某化工厂的废液经测定得知主要含有乙醇,其中还溶有苯酚(熔点:43℃)、乙酸。现欲从废液中回收它们,根据各物质的熔点和沸点,该工厂设计了以下回收的实验方案。

请回答:
(1)试剂B、C的化学式为:B ,C ;
(2)操作D的名称为: ;操作E的名称为: ;
(3)回收物的结构简式为: ;
(4)写出向G中加入试剂B反应的离子方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com