
题目列表(包括答案和解析)
5.标准状况下,下列物质中含氢原子个数最多的是
A.3.01×1024个H2分子 B.22.4 L H2O C.23 g C2H5OH D.22.4 L NH3
4.下列叙述错误的是
A.0.012kg12C中含有约6.02×1023个碳原子
B.1mol任何物质都含有约6.02×1023个原子
C.在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类
D.物质的量是国际单位制中七个基本物理量之一
3.过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
下列操作顺序不合理的是
A.③②①⑤④ B.③①②⑤④ C.②③①⑤④ D.①③②④⑤
2.浓度为2mol/L的NaOH溶液的正确含义是
A.在2L水中溶有80克的NaOH B.80克NaOH溶于2L水配成的溶液
C.每升溶液中含有80克NaOH D.每2L溶液中含有80克NaOH
1.某有机物叫苯酚。其试剂瓶上有如下标识:


上述标志的含义是
A.自然物品、易燃 B.腐蚀性、有毒 C.爆炸性、腐蚀性 D.氧化剂、有毒
22.(5分)将
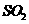 与
与 放入4L的密闭容器中,在一定条件下反应达到平衡:
放入4L的密闭容器中,在一定条件下反应达到平衡:
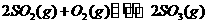 测得平衡时混合物总的物质的量为5mol,求:
测得平衡时混合物总的物质的量为5mol,求:
(1)
平衡时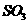 的浓度;
的浓度;
(2) 该温度下的平衡常数;
(3)
平衡时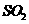 的转化率
的转化率

21.(8分)氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1g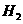 完全燃烧生成液态水,放出142.9k热量。则
完全燃烧生成液态水,放出142.9k热量。则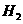 燃烧热的化学方程式为:
燃烧热的化学方程式为:
(2)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:

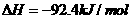
①当合成氨反直达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反
应速率与时间的关系如下图所示。
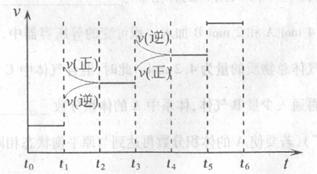
图中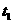 时引起平衡移动的条件可能是
时引起平衡移动的条件可能是
其中表示平衡混合物中 的含量最高的一段时间是
的含量最高的一段时间是
②温度为 °C时,将2amolH
°C时,将2amolH 和amolN
和amolN 放入0.5L密闭容器中,充分反应后测得
放入0.5L密闭容器中,充分反应后测得
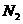 的转化率为50%,则反应的平衡常数为
的转化率为50%,则反应的平衡常数为
0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于
(2)A的转化率为
(3)生成D的反应速率为
(4)如果增大反应体系的压强,则平衡体系中C的质量分数 (填)
(5)在此温度下,该化学反应的平衡常数为
(6)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4/3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入 物质 mol
20.(14分)在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,
发生如下反应:3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡状态, 生成了
xC(g)+2D(g),2min末反应达到平衡状态, 生成了
19.(12分)有如下化学反应: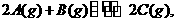
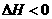
(1)若将4 mol A和2 mol B在2 L的容器中混合, 经2 s后测得C的浓度为0.6
mol/L,用物质A表示的平均反应速率为 ;2s时物质B的浓
度为 ;
(2)若把a mol A和b mol B充入一密闭容器中,达到平衡时它们的物质的量满足:
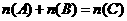 ,则A的转化率为
;
,则A的转化率为
;
(3)若将4 mol A和2 mol B加入体积可变的等压容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2 mol。此时,混合气体中C的体积分数为
;若再通入少量B气体,体系中A的体积分数 (填“增大”、“减小”
或“不变”),若要使A的体积分数再达到与原平衡状态相同。可采取的措施有
.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com