
题目列表(包括答案和解析)
7.一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)==H2(g)+I2(g)。若c(HI)由0.1 mol·L-1降到0. 07 mol·L-1时,需要15 s,那么c(HI)由0. 07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为( )
A.等于5 s B.等于10 s
C.大于10 s D.小于l0 s
6.一定温度下,可逆反应2NO2===2NO+O2在体积固定的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
A.①④⑤⑥ B.①②③⑤
C.②③④⑥ D.以上全部
5.在一恒定容积的容器中充入4 mol A和2 mol B发生如下反应:2A(g)+B(g)== xC(g),达到平衡后,C的体积分数为W%。若维持容积和温度不变,按1.2 mol A、0.6 mol B和2.8 mol C为起始物质,达到平衡后,C的体积分数仍为W%,则x的值为( )
A.只能为2 B.只能为3
C.可能为2,也可能为3 D.无法确定
4.对可逆反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x molNH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速减小,逆反应速率增大
D.化学反应速率关系是2v正(NH3)= 3v正(H2O)
3.合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)== 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )
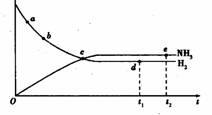
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比图中d点的值大
2.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量 ②1molCl2分子中化学键断裂时需要吸收243kJ的能量 ③由H原子和C1原子形成1 mol HC1分子时释放431 kJ的能量。下列叙述正确的是( )
A氢气和氯气反应生成氯化氢气体的热化学方程式是
H2(g)+C12(g)= 2HC1(g)
B氢气和氯气反应生成2 mol氯化氢气体,反应的△H= 183 kJ·mol-1
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H= -183 kJ·mol-1
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H= -183 kJ·mol -1
1.下列叙述正确的是( )
A.O2和O3互为同素异形体,性质相似
B.常温下,PH=1的水溶液中,Na+、NO3-、HCO3-、Fe2+可以大量共存
C.明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理相同
D.C(石墨,s)=C(金刚石,s);△H>0,所以石墨比金刚石稳定
24.(6分)在T℃时,取一定量食盐的饱和溶液用惰性电极进行电解,当阳极析出2.24L气体(标准状况)时,食盐完全电解,所得溶液的质量为36.9 g ,并测得其密度为1.20g/cm3,试计算:(1) 电解后溶液中溶质的物质的量浓度?(2) T℃时食盐的溶解度是多少?(已知原子量:Na-23,Cl-35.5)
23.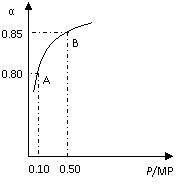 (8分)二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。(1)硫酸生产中,SO2催化氧化成SO3:2SO2(g)+O2(g)
(8分)二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。(1)硫酸生产中,SO2催化氧化成SO3:2SO2(g)+O2(g)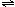 2SO3(g);某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如右图所示。根据图示回答下列问题:
2SO3(g);某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如右图所示。根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。该反应的平衡常数等于 。
②平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ·mol-1
若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为 (阿伏伽德罗常数用NA表示),放出的热量为 kJ。
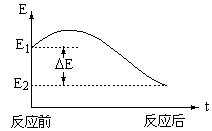
22. (6分)下图是不饱和烃加氢时能量变化示意图,具体数据如下
|
反应 |
DE |
|
CH3CºCCH3+2H2®CH3(CH2)2CH3 |
278KJ/mol |
|
CH2=CH-CH=CH2+2H2®
CH3(CH2)2CH3 |
239KJ/mol |
 (化学反应总是向能量降低的方向进行)
(1)如果CH3CH2CºCCH2CH2CH=CH-CH=CH21mol与H22mol作用,其主要产物是
(化学反应总是向能量降低的方向进行)
(1)如果CH3CH2CºCCH2CH2CH=CH-CH=CH21mol与H22mol作用,其主要产物是
(2)如果CH3CHBrCHBrCH3与NaOH的醇溶液共热后,主要产物是A,则A的结构简式为 ,另一副产物是B。
(3)若反应(2)是吸热反应,试画出A与B的能量变化差异的示意图
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com