
题目列表(包括答案和解析)
7.一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是:
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是:
A. 2 mol C B. 2 mol A 1 mol B和1 mol He(不参加反应)
C. 1 mol B和1 mol C D. 2 mol A 3 mol B和3 mol C
6.pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,
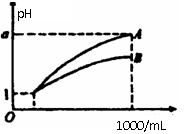 下列说法不正确的是(
)
下列说法不正确的是(
)
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
5.在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A. 1∶9 B. 1∶1 C. 1∶2 D. 1∶4
4.下列各组热化学方程式程中,化学反应的△H前者大于后者的是
①C(s)+O2(g)=CO2(g);△H1 C(s)+1/2O2(g)=CO(g);△H2
②S(s)+O2(g)=SO2(g);△H3 S(g)+O2(g)=SO2(g);△H4
③H2(s)+1/2O2(g)=H2O(g);△H5 H2(g)+O2(g)=2H2O(l);△H6
④CaCO3(s)=CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)=Ca(OH)2(s);△H8
A. ① B. ④ C. ②③④ D. ①②③
3.在2L密闭容器中加入4molA和6molB,发生以下反应:4A(g)+6B(g)  4C(g) +5D(g)。若经5s后,剩下的A是2.5mol,则B的反应速率是
4C(g) +5D(g)。若经5s后,剩下的A是2.5mol,则B的反应速率是
A.0.45 mol / (L•s)) B.0.15 mol /(L•s))
C.0.225 mol /(L•s) D.0.9 mol /(L•s))
2.100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃
的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g)
 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2 ②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化 ④烧瓶内气体的质量不再变化 ⑤NO2的物质的量浓度不再改变 ⑥烧瓶内气体的颜色不再加深 ⑦烧瓶内气体的平均相对分子质量不再变化 ⑧烧瓶内气体的密度不再变化。
A.②③⑥⑦ B.①④⑧ C.只有①④ D.只有⑦⑧
1.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l) + 3/2O2(g) == CO2(g) + 2H2O(l);△H=+725.8kJ/mol
B.2CH3OH(l) + 3O2(g) == 2CO2(g) + 4H2O(l);△H=-1452kJ/mol
C.2CH3OH(l) + 3O2(g) == 2CO2(g) + 4H2O(l);△H=-725.8kJ/mol
D.2CH3OH(l) + 3O2(g) ==2 CO2(g) + 4H2O(l);△H=+1452kJ/mol
2.(6分) 铁在热的稀HNO3中反应,其主要还原产物为N20,而在冷的稀HN03中反应,其主要还原产物为
NO,当溶液更稀时,其主要还原产物是NH4+请分析下图,回答有关问题。 .

(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时反应的化学方程式:
□Fe+□HN03 ====□Fe(N03)3+□□+□H2O
(2)判断从O点到a点时的还原产物,应为
(3)a到b点时产生还原产物为 ,其原因是
(4)已知到达d点时反应完全结束,此时溶液中的主要阳离子为 。 分析c点与d点投入金属铁的物质的量之比n(c)/ n(d) == .

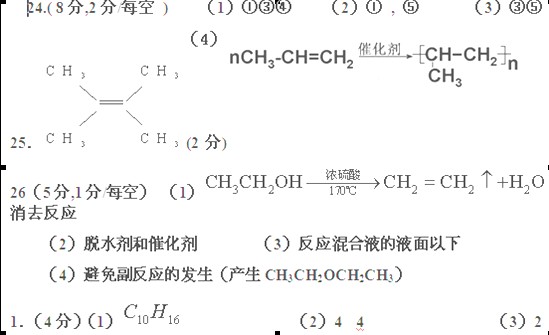

1. (4分)有的油田开采的石油中溶有一种碳氢化合物--金刚烷,
(4分)有的油田开采的石油中溶有一种碳氢化合物--金刚烷,
它的分子立体结构如图所示:
(1)由图可知其分子式为:____________。
(2)它是由_________个六元环构成的六体的笼状结构,
其中有__________个碳原子为三个环共有。
(3)金刚烷分子的一氯代物有_______种。
26.(5分) 简答实验室制乙烯的有关问题:
(1)写出反应的化学方程式,并指出反应类型。
(2)反应中浓硫酸起什么作用?
(3)气体发生装置中的温度计应插入在什么部位?
(4)实验中为什么要使温度迅速升高到170℃?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com