
题目列表(包括答案和解析)
26.(1) 酸 , 略
(2) 3 ; 5 (填序号)
(3)② > ③(填“>” “<”或“=”)(4) = =
(5) 略
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
A |
B |
B |
D |
C |
C |
B |
B |
C |
D |
A |
D |
A |
|
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
|
|
D |
A |
C |
A |
B |
A |
C |
C |
D |
A |
B |
C |
|
30.(5分)在VmLBaCl2溶液中,加入一定体积0.05mol/L的H2SO4溶液中,恰好完全反应,测得反应后溶液的PH=3,求原BaCl2溶液的物质的量浓度(忽略溶液体积的变化).
高二化学
29.(8分).如果溶液中C(Ag+)C(Cl-)的乘积是一个常数:1.0×10-10
(1)500mL0.018mol/L的AgNO3溶液中加入500mL0.018mol/L盐酸,生成沉淀后溶液中C(Ag+)= 。
(2)向500mL0.018mol/L AgNO3的溶液中加入50mL0.02 mol/L的盐酸,生成了沉淀后溶液中的C(Ag+)是多少?求溶液的pH
28.
 选酚酞作指示剂,用中和滴定法测定烧碱样品的纯度(所含杂质不与盐酸反应)。试根据实验回答:
选酚酞作指示剂,用中和滴定法测定烧碱样品的纯度(所含杂质不与盐酸反应)。试根据实验回答:
(1)准确称取4.8g烧碱样品,所用仪器除了药匙,烧杯外,还需有 。
(2)将已称好的样品配成250 mL待测液,需要的仪器除了烧杯,玻璃棒还有 。
(3)用0.2000 mol / L标准盐酸滴定待测烧碱溶液,滴定时边滴边摇动锥形瓶,两眼注视 ,直到滴定终点。
(4)判断到达滴定终点的实验现象是 。 (5)根据下列数据计算,待测烧碱溶液的浓度为 。(计算结果保留四位有效数字)
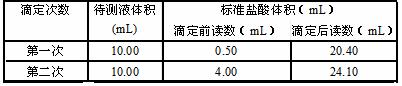
(6)根据上述数据计算,烧碱样品的纯度为
(7) ① 滴定过程中,锥形瓶用蒸馏水洗涤后,水未倒尽,则测得烧碱样品的纯度 (填“偏高”, “偏低”或“无影响”)
②滴定前仰视,滴定后俯视,则测得烧碱样品的纯度 (填“偏高”, “偏低”或“无影响”)
27. (7分) 已知氮化钠(Na3N)在熔融时能导电,与水作用时有NH3产生。试回答下列问题:
(1)氮化钠属于____________(选“共价”“离子”)化合物。
(2)比较粒子的半径:Na+ _________N3-(填“>”、“<”、“=”)
(3)Na3N与水反应的化学方程式是______________________________________
26.(18分)在常温下,下列五种溶液:
①0.1mol/L ②0.1mol/L
②0.1mol/L ③0.1mol/L
③0.1mol/L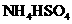
④0.1mol/L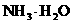 和0.1mol/L
和0.1mol/L 混合液 ⑤0.1mol/L
混合液 ⑤0.1mol/L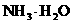
请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是
(用离子方程式表示)
(2)在上述五种溶液中,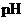 最小的是 ;
最小的是 ; 最小的是 (填序号)
最小的是 (填序号)
(3)比较溶液②、③中 的大小关系是② ③(填“>” “<”或“=”)
的大小关系是② ③(填“>” “<”或“=”)
(4)常温下,测得溶液②的 ,则说明
,则说明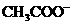 的水解程度 (填“>”、“<”或“=”)
的水解程度 (填“>”、“<”或“=”) 的水解程度,
的水解程度,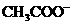 与
与 浓度的大小关系是:
浓度的大小关系是: 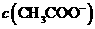
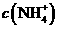 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(5)请写出③的电离方程式: 。
25.醋酸是弱电解质,下列性质中不能说明它是弱电解质的是( )
A.1.0 mol·L-1醋酸溶液pH约为2
B.pH=3的醋酸溶液加水稀释100倍后,其pH<5
C.10 mL1.0 mol·L-1醋酸溶液恰好与10 mL 1.0 mol·L-1氢氧化钠溶液完全反应
D.醋酸钠为强电解质+
24.25℃时,将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:100混合,反应后所得溶液pH=7。若x= y/3,则x值为 ( )
A.2 B.3 C.4 D.5
23.当用标准盐酸溶液滴定待测氢氧化钠溶液时,下列操作中会使测定结果偏低的是
A.用酸式滴定管滴至终点时,俯视滴定管读数
B.将碱液移入锥形瓶后,加了10 ml蒸馏水再滴定
C.酸式滴定管用蒸馏水润洗后,未用标准盐酸溶液润洗
D.酸式滴定管注入酸液时,尖嘴处留有气泡,达滴定终点时气泡消失
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com